
Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Amyloidose der Leber
Facharzt des Artikels
Zuletzt überprüft: 29.06.2025
Amyloidose ist in der Regel eine systemische, allgemeine Erkrankung, die durch die Ansammlung von Amyloid (einem spezifischen Glykoprotein) im Gewebe und die daraus resultierende Störung der normalen Organfunktion gekennzeichnet ist. Leberamyloidose ist deutlich seltener als Nieren- und Milzamyloidose [ 1 ], geht aber fast immer mit systemischen Schäden einher. Keines der bestehenden bildgebenden Verfahren kann Amyloid spezifisch nachweisen. Selbst bei klinischem und radiologischem Verdacht ist die Diagnose einer Amyloidose auf eine Gewebebiopsie angewiesen, um das Vorhandensein von Amyloidablagerungen zu bestätigen. [ 3 ] Die Behandlung ist komplex und umfassend und umfasst immunsuppressive und symptomatische Maßnahmen. In schweren Fällen kann eine Lebertransplantation erforderlich sein.
Epidemiologie
Der Behandlungserfolg hängt direkt von der rechtzeitigen Diagnose der Erkrankung ab, die zur Bildung eines Protein-Polysaccharid-Komplexes (Amyloid) in verschiedenen Organen und der Leber führt. Wie die Praxis zeigt, ist eine Amyloidose schwer anzunehmen oder zu vermuten, obwohl sie identifiziert und bestätigt werden kann. Tatsächlich ist die Krankheit in über 80 % der nicht erkannten Fälle klinisch durch eine Lebererkrankung maskiert. Die effektivste Diagnosemethode ist die Biopsie.
Leberamyloidose ist im Vergleich zur Nierenamyloidose seltener. Gleichzeitig gehen alle Fälle von Leberschädigungen mit Schädigungen anderer Organe einher. Am häufigsten betrifft die Pathologie vorwiegend strukturelle Teile der Lebertrias, was die minimale und unspezifische Symptomatik bestimmt. Das klinische und morphologische Bild des hepatozellulären Mangels und der portalen Hypertonie manifestiert sich in diffusen und intralobulären Formen der Pathologie.
Eine Leberbiopsie ist gerechtfertigt, wenn eine Hepatomegalie ohne vorherige Lebersymptome vorliegt und kein nephrotisches Syndrom vorliegt.
Eine diffuse Leberbeteiligung ist in etwa 25 % der Fälle zu beobachten, bei 75 % der Patienten sind nur die Pfortadern betroffen.
Bei der primären Amyloidose ist in 90 % der Fälle die Leber betroffen, bei der sekundären Amyloidose hingegen nur in 47 % der Fälle.
Eine isolierte Leberbeteiligung ist äußerst selten. Nieren (ca. 93 % der Fälle), Milz (72 %), Herz (57 %), Bauchspeicheldrüse (36 %), Nebennieren (29 %), Darm und Lunge (je 21 %) sind meist gleichzeitig betroffen.
Frauen erkranken fast doppelt so häufig wie Männer. Die durchschnittliche Lebenserwartung von Amyloidose-Patienten beträgt 52–64 Jahre.
Ursachen hepatische Amyloidose
Amyloidose verläuft mit der Bildung und Ansammlung eines komplexen Polysaccharid-Protein-Komplexes – Amyloid – im Lebergewebe. Das Problem des Auftretens der primären Läsion ist bisher unzureichend untersucht. Was die sekundäre Pathologie betrifft, so ist ihr Auftreten üblicherweise mit solchen Krankheiten verbunden:
- Chronische Infektionsprozesse (Tuberkulose, Syphilis, Aktinomykose);
- Eitrige Entzündungsprozesse (mikrobielle Endokarditis, Osteomyelitis, Bronchiektasien usw.);
- Bösartige Erkrankungen (Leukämie, viszeraler Krebs, Lymphogranulomatose).
Die reaktive Form der Amyloidose tritt bei Patienten mit begleitender Arteriosklerose, rheumatischen Erkrankungen (Morbus Bechterew, rheumatoide Arthritis), Psoriasis, chronischen Entzündungen und Multisystemerkrankungen (einschließlich Sarkoidose) auf. Die wichtigsten Risikofaktoren sind: erbliche Veranlagung, zelluläre Immunitätsstörungen, Hyperglobulinämie.
Pathogenese
Es gibt eine Reihe von Annahmen über den Ursprung der Leberamyloidose. Die meisten Spezialisten vertreten die Ansicht, dass die Erkrankung auf Dysproteinose, immunologischen und mutationsbedingten Ursachen sowie einer lokalen zellulären Genese beruht. Die zelluläre Genese umfasst Veränderungen in Reaktionen auf zellulärer Ebene (Bildung fibrillärer Amyloidvorläufer durch einen Makrophagenkomplex), obwohl Amyloid außerhalb der Zellstrukturen gebildet und akkumuliert wird.
Die Dysproteinose-Variante basiert auf der Tatsache, dass Amyloid ein Produkt eines fehlerhaften Proteinstoffwechsels ist. Die grundlegende pathogenetische Verbindung des Problems liegt in Dysproteinämie und Hyperfibrinogenämie, die zur Ansammlung grob verteilter Protein- und Paraproteinfraktionen im Plasma führen.
Nach der immunologischen Theorie wird die Amyloidbildung durch eine Antigen-Antikörper-Reaktion verursacht, bei der Gewebezerfallsprodukte oder Fremdproteine als Antigene wirken. Amyloidakkumulation findet sich vor allem im Bereich der Antikörperbildung und des übermäßigen Vorhandenseins von Antigenen.
Für die plausibelste Version halten Wissenschaftler die Mutationstheorie, die eine Vielzahl mutagener Faktoren berücksichtigt, die zu Anomalien bei der Proteinsynthese führen können.
Amyloid ist ein komplexes Hypoprotein, das aus globulären und fibrillären Proteinen und Polysacchariden besteht. Amyloidansammlungen beeinträchtigen die Intima und Adventitia des Gefäßsystems, das Stroma parenchymatöser Organe, die Drüsenstruktur usw. Amyloidansammlungen verursachen keine Funktionsschäden. Kleinere Ansammlungen verursachen keine Funktionsstörungen, doch bei starkem Amyloidbefall in der Leber nimmt das Volumen zu, verändert das Erscheinungsbild des Organs und es entwickelt sich ein Funktionsverlust.
Die Leberamyloidose ist durch die Ablagerung von Amyloidfibrillen im Dysse-Raum gekennzeichnet, die normalerweise im periportalen Bereich beginnt, obwohl sie manchmal zentrilobulär ist und sich auch in den Lebergefäßen ablagern kann. [ 4 ], [ 5 ] In schweren Fällen führt die Amyloidablagerung zu einer Druckatrophie der Hepatozyten, die den Gallendurchgang verhindert und zu Cholestase führt, oder die Sinusoide blockieren kann, was zu portaler Hypertonie führt. [ 6 ], [ 7 ], [ 8 ]
Symptome hepatische Amyloidose
Das klinische Bild der Leberamyloidose ist vielfältig und hängt von der Intensität der Amyloidansammlung, ihren biochemischen Eigenschaften, der Dauer des pathologischen Prozesses, dem Grad der Organschädigung und der Beeinträchtigung ihres Funktionszustands ab.
Im latenten Stadium der Amyloidose, wenn Amyloidansammlungen in der Leber nur durch mikroskopische Untersuchung nachgewiesen werden können, fehlen die ersten Anzeichen der Krankheit. Mit der weiteren Entwicklung und zunehmendem Funktionsdefizit des Organs schreitet die Symptomatik fort.
Die Leber verdickt sich allmählich und vergrößert sich. Durch Palpation lassen sich veränderte, aber glatte und schmerzlose Ränder des Organs ertasten. Selten geht die Pathologie mit Schmerzen im subkostalen Bereich rechts, Dyspepsie, Milzvergrößerung, Gelbfärbung der Haut, Schleimhäute und Skleren sowie einem hämorrhagischen Syndrom einher.
Die charakteristischsten Symptome bei Leber-Amyloidose: [ 9 ], [ 10 ]
- Eine Amyloidansammlung in der Leber führt bei 33–92 % der Patienten zu einer Hepatomegalie.
- Leichte Gelbsucht
- Portale Hypertonie;
- Mittelschwere bis schwere Cholestase.
Da Amyloidose nur sehr selten nur ein Organ betrifft, treten in der Regel weitere Symptome auf:
- Bei Nierenschäden kommt es zu einem nephrotischen Syndrom und arterieller Hypertonie mit anschließendem Nierenversagen, Ödemen, manchmal Nierenvenenthrombose, Leukozyturie, Hämaturie, Hypoproteinämie, Azotämie usw.;
- Wenn das Herz betroffen ist, entwickelt sich ein Zustand ähnlich der restriktiven Kardiomyopathie (Rhythmusstörungen, Kardiomegalie, zunehmendes Herzversagen, Schwäche und Atemnot, Ödeme, seltener Flüssigkeitsansammlung in der Bauch- und Pleurahöhle, Perikarditis).
- Wenn der Verdauungstrakt betroffen ist, können Makroglossie, Schwäche und Peristaltik der Speiseröhre, Übelkeit und Sodbrennen, Verstopfung oder Durchfall usw. auftreten.
- Wenn die Bauchspeicheldrüse betroffen ist, treten die Symptome einer chronischen Pankreatitis auf.
- Bei einer Beteiligung des Bewegungsapparates kommt es zu symmetrischer Polyarthritis, Karpaltunnelsyndrom und Myopathien, bei einer Beteiligung des Nervensystems zu Polyneuropathien, Lähmungen, orthostatischem Blutdruck, vermehrtem Schwitzen und Demenz.
Wenn sich die pathologische Reaktion auf die Haut ausbreitet, erscheinen zahlreiche wachsartige Plaques im Gesicht, am Hals und in Hautfalten. Das Bild von Neurodermitis, rotem Plattenepithelfieber und Sklerodermie ist möglich.
Die Kombination mehrerer Amyloidläsionen und die Vielfalt der Symptome erschweren die Identifizierung einer Leberamyloidose erheblich und erfordern eine umfassende und vollständige Diagnose.
Formen
Nach der WHO-Klassifikation werden fünf Arten der Amyloidose unterschieden:
- AL (primär);
- AA (Sekundarstufe);
- ATTR (hereditär und senil systemisch);
- Aβ2M (bei Patienten unter Hämodialyse);
- AIAPP (bei Patienten mit insulinunabhängigem Diabetes mellitus);
- AB (für Alzheimer-Krankheit);
- AANF (senile Vorhofamyloidose).
Es liegt eine lokale Amyloidose der Leber vor, häufiger handelt es sich jedoch um eine systemische Läsion, bei der der pathologische Prozess auch die Nieren, das Herz, die Milz, das Nervensystem sowie andere Organe und Gewebe betrifft.
Komplikationen und Konsequenzen
Systemische Amyloidose führt allmählich zur Entwicklung akuter pathologischer Prozesse, die wiederum zum Tod führen können. Zu den häufigsten und lebensbedrohlichsten Komplikationen gehören:
- Häufige infektiöse (bakterielle, virale) Pathologien, einschließlich Lungenentzündung, Pyelonephritis, Glomerulonephritis;
- Chronisches Leber- und Nierenversagen;
- Chronische Herzinsuffizienz (kann einem Herzinfarkt vorausgehen);
- Hämorrhagische Schlaganfälle.
Eine Venenthrombose entsteht durch die Ansammlung und Ablagerung von Proteinen an den Venenwänden. Das Lumen der betroffenen Gefäße verengt sich, es kommt zu Organversagen. Im Laufe der Zeit kann sich das Gefäß vor dem Hintergrund einer langfristigen Hyperproteinämie vollständig verschließen. Jede dieser Komplikationen kann zu einem ungünstigen Ausgang führen – dem Tod.
Diagnose hepatische Amyloidose
Bei Verdacht auf Leberamyloidose werden nach obligatorischen Konsultationen diagnostische Maßnahmen durchgeführt, sowohl beim Gastroenterologen und Therapeuten als auch beim Rheumatologen, Kardiologen, Dermatologen, Neurologen und Urologen. Es ist wichtig, die Daten der Anamnese und der klinischen Manifestationen umfassend auszuwerten und eine umfassende Labor- und Instrumentendiagnostik durchzuführen.
Die Untersuchungen umfassen notwendigerweise Urin- und Blutuntersuchungen. Bei hepatischer Amyloidose findet sich häufig eine Kombination aus Leukozyturie mit Proteinurie und Zylindrurie sowie Hypoproteinämie – mit Hyperlipidämie, Anämie, Hyponatriämie und Hypokalzämie, reduzierter Thrombozytenzahl. Paraproteine werden in der Urin- und Serumelektrophorese nachgewiesen.
Zur instrumentellen Diagnostik gehören:
- EKG, Echo;
- Ultraschall des Bauchraums;
- Röntgenaufnahmen des Magens, der Speiseröhre;
- Irrigographie, Bariumröntgenaufnahme;
- Endoskopie.
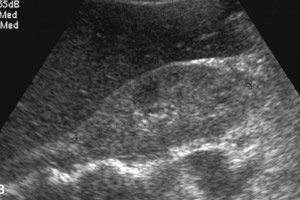
Radiologische Befunde einer hepatischen Amyloidose umfassen eine unspezifische Hepatomegalie, erhöhte Echogenität im Ultraschall oder Dichte in der Computertomographie (CT) und erhöhte T1-Signalintensität in der Magnetresonanztomographie (MRT). [ 12 ] Die Szintigraphie mit Tc-99m-verwandten Indikatoren zeigt eine heterogene Aufnahme, diese ist jedoch unspezifisch. [ 13 ], [ 14 ] Es wurde gezeigt, dass GC die mittelsElastographie gemessene Lebersteifigkeit erhöht; [ 15 ], [ 16 ], [ 17 ], es gibt jedoch nur wenige Fallberichte. Die Magnetresonanz-Elastographie (MRE) ist derzeit die zuverlässigste nichtinvasive Methode, um eine Leberfibrose zu erkennen und in ihr Stadium zu unterteilen, [ 18 ], [ 19 ]. Die MRE ist nützlich, um das Fortschreiten der Erkrankung, das Ansprechen auf die Behandlung und die Vorhersage einer Leberdekompensation bei Patienten mit Leberfibrose zu erkennen. [ 20 ]
Eine Amyloidose der Leber ist im Ultraschall schwer zu bestimmen: Es wird eine Vergrößerung des Organs festgestellt, wobei die spezifischste Hepatomegalie 15 cm überschreitet. Unter Ultraschallkontrolle wird eine Biopsie durchgeführt, die als entscheidender Indikator für die Diagnose dient. Mit einer speziellen Nadel wird eine kleine Menge Lebergewebe entnommen, anschließend mit einem speziellen Farbstoff angefärbt und unter dem Mikroskop untersucht, wodurch Amyloidablagerungen direkt sichtbar werden.
Eine definitive Diagnose wird erst nach dem Nachweis von Amyloidfibrillen im Gewebe der Leber und anderer Organe gestellt. Der genetisch bedingte Typ der Amyloidose wird durch eine sorgfältige genetisch-medizinische Untersuchung des Stammbaums festgestellt.
Differenzialdiagnose
Bei allen Patienten mit einer Kombination aus renaler Proteinurie, restriktiver Kardiomyopathie, autonomer oder peripherer Neuropathie und Hepatomyelie sollte eine Amyloidose vermutet werden, auch wenn kein monoklonales Paraprotein vorliegt. Die Überprüfung des Amyloidosetyps ist sehr wichtig, da die Behandlung von Läsionen unterschiedlicher Ätiologie sehr unterschiedlich ist.
Die histologische Diagnostik erfolgt durch Färbung mit Kongorot und anschließende mikroskopische Untersuchung unter polarisierendem Licht. Es empfiehlt sich, mehrere Gewebeproben gleichzeitig zu biopsieren. Bei positivem Färbeergebnis wird eine immunhistochemische Analyse mit monoklonalen Antikörpern gegen Vorläuferproteine durchgeführt, um den Amyloidtyp zu identifizieren.
Mithilfe einer DNA-Analyse lässt sich zwischen primärer Amyloidose und verschiedenen Varianten einer genetisch bedingten Amyloidose unterscheiden. Amyloidfibrillen können aus Biopsieproben isoliert und in einzelne Aminosäuren zerlegt werden.
Zusätzliche Untersuchungen zur Feststellung einer Plasmazelldyskrasie:
- Elektrophorese von Serumproteinen von Blut und Urin;
- Immunassay für freie Leichtketten;
- Immunofixierung (Immunoblotting) von Serumproteinen;
- Knochenmarkaspiration und Trepanobiopsie.
Die Diagnose einer Leberamyloidose ist ein langwieriger und arbeitsintensiver Prozess, der erhöhte Aufmerksamkeit von Spezialisten und hochwertige Ausstattung von Kliniken und Laboren erfordert.
Wen kann ich kontaktieren?
Behandlung hepatische Amyloidose
Die Behandlungsmaßnahmen zielen darauf ab, die Konzentration bereits vorhandener Amyloidproteine im Blut zu senken (Beseitigung der Ursache der Amyloidose) und eine ausreichende Leberfunktion zu unterstützen.
Sekundäre Amyloidose erfordert die Blockierung des Entzündungsprozesses (bei chronischen Infektions- und Autoimmunerkrankungen). Bei Autoimmunerkrankungen wird der Einsatz von Zytostatika empfohlen. Um chronische Infektionsprozesse zu eliminieren, wird der Entzündungsbereich häufig chirurgisch entfernt. Oft kann dieser Ansatz das weitere Fortschreiten der Amyloidose stoppen und die Leberfunktion verbessern.
Bei primärer Amyloidose ist der Einsatz chemopräventiver Medikamente und manchmal eine Knochenmarktransplantation erforderlich.
Aktuelle Leitlinien empfehlen die Kombination von Cyclophosphamid, Bortezomib, Dexamethason (CyBorD) und Daratumumab als Erstlinientherapie bei Patienten mit neu diagnostizierter AL.
Bortezomib ist ein Proteasominhibitor. Proteasomen sind an der Reduzierung der Proteotoxizität und der Regulierung von Proteinen beteiligt, die die Zellprogression und Apoptose steuern. Plasmazellen, die Amyloid produzieren, reagieren besonders empfindlich auf die Proteasomhemmung, da sie auf das Proteasom angewiesen sind, um die toxischen Effekte von Leichtketten zu reduzieren und Apoptose zu verhindern.
Daratumumumab ist ein monoklonaler Antikörper (mAb), der an CD38 bindet, ein transmembranäres Glykoprotein auf der Oberfläche von Plasmazellen, das Apoptose induziert. Es ist das einzige Medikament, das speziell für die Behandlung der AL-Amyloidose in Kombination mit CyBorD zugelassen ist. Die Wirksamkeit von CyBorD-Daratumumumab ist sehr hoch: 78 % der Patienten erreichten eine signifikante hämatologische Remission (definiert als vollständige Remission oder sehr gute partielle Remission). Die mediane Überlebenszeit in der kleinen Gruppe der Patienten, die CyBorD erhielten (n = 15), betrug 655 Tage, verglichen mit 178 Tagen bei Patienten, die eine andere Melphalan-Dexamethason-basierte Behandlung erhielten (n = 10).
Allerdings sind mit diesen Therapien zahlreiche Nebenwirkungen verbunden, darunter Kardiotoxizität, die eine Dosisreduktion oder ein Absetzen der Behandlung sowie den Einsatz anderer, weniger wirksamer, aber verträglicherer Therapiestrategien erforderlich machen.
Isatuximab, ein monoklonaler Antikörper gegen CD38 ähnlich wie Daratumumab, wird zur Behandlung der Plasmazelldyskrasie untersucht, die AL zugrunde liegt.
Drei monoklonale Antikörper – Birtamimab, CAEL-101 und AT-03 – werden derzeit auf ihre Wirksamkeit bei der Entfernung von Amyloidfibrillen aus erkrankten Organen untersucht. Die Ergebnisse dieser Studien werden direkte Belege für die Hypothese liefern, dass die Entfernung von Leichtketten-Ablagerungsfibrillen aus Organen zu einer Verbesserung der Organfunktion führt. [ 21 ]
Zur Unterstützung der Leberfunktion werden Medikamente auf Basis von Ursodesoxycholsäure verschrieben (z. B. Ursosan). Ursodesoxycholsäure trägt zur Stabilisierung der Zellmembranen bei, reduziert die negativen Auswirkungen toxischer Fettsäuren auf die durch Amyloidablagerungen verursachte Gallenstauung und trägt zur Wiederherstellung des normalen Gallenabflusses bei.
Darüber hinaus erfolgt eine symptomatische Therapie und die Unterstützung der Funktion anderer lebenswichtiger Strukturen wie Nervensystem, Herz, Nieren usw. Die unterstützende Therapie für Patienten mit hepatischer Amyloidose umfasst verschiedene klinische Aspekte, darunter die Behandlung von Herzinsuffizienz, Arrhythmien, Reizleitungsstörungen, Thromboembolien und dem gleichzeitigen Vorliegen einer Aortenstenose.
Andere Behandlungen hängen von der Art der Amyloidose und den betroffenen Körperteilen ab. Zu den Behandlungen können gehören: [ 22 ]
- Arzneimittel zur Linderung der Symptome, wie Schmerzmittel, Mittel gegen Übelkeit oder Arzneimittel zur Verringerung von Schwellungen (Diuretika);
- Medikamente zur Reduzierung von Amyloid;
- Nierendialyse;
- Lebertransplantation.
Die Leber produziert 95 % des im Serum gemessenen TTR (Transthyretin, ein Protein, das am Thyroxin(T4)-Transport und Retinol-bindenden Protein beteiligt ist. Transthyretin wird hauptsächlich in der Leber synthetisiert und ist reich an Beta-Strängen, die dazu neigen, zu unlöslichen Amyloidfibrillen zu aggregieren). Daher wird seit 1990 eine Lebertransplantation als Erstlinientherapie zur Beseitigung der Hauptquelle amyloidogenen TTR bei Patienten mit der familiären Form (ATTRv) empfohlen, während sie bei der ATTR-wt-Form nicht angezeigt ist. Eine Lebertransplantation bei jungen Patienten in den Frühstadien der Erkrankung ist mit einer hohen 20-Jahres-Überlebensrate verbunden. Bei manchen Mutationen scheint eine Lebertransplantation wirksamer und bei anderen, wie z. B. V122I (assoziiert mit Kardiomyopathie), weniger wirksam zu sein. Bei jungen ATTRv-Patienten mit Kardiomyopathie ist auch eine kombinierte Leber- und Herztransplantation möglich und Literaturdaten zu einer kleinen Patientengruppe legen nahe, dass diese Kombination eine bessere Prognose hat als eine Herztransplantation allein.
Bei Patienten mit hepatischer Amyloidose ist die Einnahme von Herzglykosiden und Kalziumantagonisten wie Diltiazem oder Verapamil kontraindiziert, da diese sich im Amyloid anreichern können. ACE-Hemmer und Betablocker sind mit Vorsicht anzuwenden.
Bei orthostatischer Hypotonie werden Mineralokortikoide oder Glukokortikosteroide verschrieben, wobei zu berücksichtigen ist, dass sie eine Dekompensation der Herzinsuffizienz verursachen können. Auch das Alpha-Adrenomimetikum Midodrin (Gutron) wird mit Vorsicht angewendet.
Bei Neuropathien sind Antikonvulsiva und Antidepressiva angebracht.
In einigen Fällen einer Leber-Amyloidose müssen Ärzte eine Organtransplantation in Betracht ziehen.
Verhütung
Aufgrund fehlender Informationen über die Pathogenese der Leberamyloidose können Spezialisten keine spezifische Prävention der Krankheit entwickeln. Daher konzentrieren sich die Hauptanstrengungen auf die rechtzeitige Erkennung und Behandlung chronischer Erkrankungen, die die Entwicklung der Erkrankung provozieren können. Bei Fällen von Amyloidose jeglicher Lokalisation in der Familie wird empfohlen, systematisch Ärzte für ambulante Untersuchungen aufzusuchen.
Im Allgemeinen beschränken sich vorbeugende Maßnahmen auf die rechtzeitige Beseitigung von Infektionskrankheiten, insbesondere solcher, die dazu neigen, sich in einen chronischen Prozess zu verwandeln. Es geht darum, die Entwicklung von Tuberkulose, Lungeninfektionen usw. zu verhindern. Wichtig ist die rechtzeitige Erkennung und angemessene Behandlung von Streptokokkeninfektionen, die chronische Formen autoimmuner Entzündungsprozesse verursachen können. Wir sprechen von Scharlach, Streptokokken-Mandelentzündung usw.
Wenn der Patient bereits an einer Autoimmunerkrankung leidet, sollte er systematisch einen Arzt konsultieren, die Aktivität der Krankheit beobachten, die erforderlichen Medikamente gemäß der ärztlichen Verordnung anwenden und die Dosierung den Indikationen entsprechend anpassen.
Prognose
Die Prognose für Patienten mit hepatischer Amyloidose ist ungünstig. Die Krankheit schreitet langsam, aber kontinuierlich voran, was schließlich zu Funktionsstörungen der betroffenen Organe und zum Tod – insbesondere durch Organversagen – führt.
Patienten mit systemischer Pathologie sterben hauptsächlich an der Entwicklung eines chronischen Nierenversagens, obwohl in einigen Fällen eine Hämodialyse oder eine kontinuierliche ambulante Peritonealdialyse die Prognose solcher Patienten verbessert. Die Überlebensrate von Patienten unter Hämodialyse, unabhängig von ihrer Art, ist mit der von Menschen mit anderen systemischen Pathologien und Diabetes mellitus vergleichbar.
Die häufigste Todesursache bei einer Hämodialyse ist die Entwicklung von Komplikationen des Herz-Kreislauf-Systems.
Die Lebertransplantation gilt seit langem als eine der wichtigsten Behandlungsmethoden der Krankheit. Die optimistischsten Überlebensraten werden bei Patienten beobachtet, deren Alter 50 Jahre nicht überschreitet (vorausgesetzt, der pathologische Prozess ist kurzlebig und der Body-Mass-Index ist normal). Patienten mit Leberamyloidose in Kombination mit peripherer Neuropathie haben eine etwas schlechtere Prognose.

