
Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Fortschreitende Atrophie des Gesichts
Facharzt des Artikels
Zuletzt überprüft: 05.07.2025
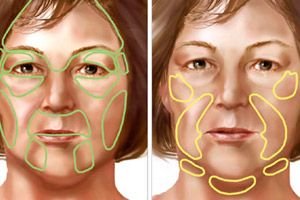
In der Literatur ist diese Krankheit unter zwei Begriffen bekannt: Hemisphärische progressive Gesichtsatrophie (Hemiatrophia faciei progressiva) und Bilaterale progressive Gesichtsatrophie (Atrophia faciei progressiva bilateralis).
Darüber hinaus kann eine hemisphärische und kreuzförmige Atrophie des Gesichts und des Körpers beobachtet werden.
Ursachen fortschreitende Gesichtsatrophie
Als mögliche Ursachen für die Erkrankung gelten Schädel- oder Gesichtsverletzungen, allgemeine oder lokale Infektionen, Syphilis, Syringomyelie, Schäden am V. oder VII. Hirnnervenpaar, Exstirpation oder Verletzung des zervikalen sympathischen Truncus usw. Einige Autoren räumen die Möglichkeit einer Hemiatrophie des Gesichts ein, kombiniert mit einer Hemiatrophie des Körpers aufgrund einer Dystrophie der diencephalen Teile des autonomen Nervensystems.
Es gibt Fälle von Hemiatrophie nach einer epidemischen Enzephalitis sowie bei Lungentuberkulose, die den zervikalen Sympathikus befallen hat.
Nach den vorliegenden Daten ist die progressive Gesichtsatrophie in der überwiegenden Mehrheit der Fälle ein Syndrom verschiedener Erkrankungen, bei denen das autonome Nervensystem auf seinen verschiedenen Ebenen am pathologischen Prozess beteiligt ist. Offensichtlich sind Traumata und andere Faktoren nur ein Anstoß für die Entwicklung dieser schwerwiegenden neurodystrophischen Phänomene.
Symptome fortschreitende Gesichtsatrophie
Die Patienten beklagen sich im Allgemeinen darüber, dass die betroffene Gesichtshälfte kleiner ist als die gesunde; der Unterschied im Volumen des Gesichtsschädels und der Weichteile nimmt allmählich zu; auf der betroffenen Seite ist die Haut dunkel-espenfarben, dünner und zieht sich beim Lächeln in viele Falten.
Manchmal bemerken die Patienten einen kribbelnden Schmerz im Bereich der betroffenen Wange oder in der gesamten Gesichtshälfte, Tränenfluss aus dem Auge der betroffenen Seite, besonders bei Kälte, im Wind und eine Veränderung der Wangenfarbe, besonders auffällig bei Kälte.
Bei schwerer Hemiatrophie erscheint es so, als gehöre die eine Gesichtshälfte einer durch Hunger oder Krebsvergiftung bis zum Äußersten abgemagerten Person, die andere Hälfte einer gesunden Person. Die Haut auf der betroffenen Seite ist gelblich-grau oder bräunlich gefärbt und errötet nicht. Die Lidspalte ist durch das Absinken des Unterlids erweitert.
Beim Druck auf die Foramina supraorbitale, infraorbitale und mentale treten Schmerzen auf.
Der Hornhautreflex ist reduziert, die Pupillen sind jedoch gleichmäßig erweitert und reagieren gleichmäßig auf Licht.
Die ausgedünnte Haut fühlt sich pergamentartig an; die Atrophie erstreckt sich auch auf das Unterhautgewebe, die Kau- und Schläfenmuskulatur sowie das Knochengewebe (Kiefer, Jochbein und Jochbogen).
Das Kinn ist zur betroffenen Seite verlagert, da die Größe des Körpers und des Unterkieferastes reduziert sind. Dies ist besonders ausgeprägt bei Patienten, die seit ihrer Kindheit an einer Hemiatrophie des Gesichts leiden. Die Hälfte der Nase ist ebenfalls reduziert, die Ohrmuschel ist faltig.
In manchen Fällen ist die Hemiatrophie des Gesichts mit einer Atrophie der gleichen Körperhälfte, manchmal auch mit einer Atrophie der gegenüberliegenden Körperseite (Hemiatrophia cruciata) verbunden, mit einseitiger Sklerodermie oder übermäßiger Pigmentablagerung in der Haut, Wachstumsstörungen oder Depigmentierung der Haare, Hemiatrophie der Zunge, des weichen Gaumens und der Alveolarfortsätze, Karies und Zahnverlust sowie Störungen beim Schwitzen.
Sobald die Hemiatrophie im Gesicht den einen oder anderen Schweregrad erreicht hat, stoppt sie, stabilisiert sich und schreitet nicht weiter fort.
Klinische und physiologische Untersuchungen dieser Patientengruppe zeigten, dass bei allen Formen der progressiven Gesichtsatrophie ausgeprägte Funktionsstörungen des autonomen Nervensystems in unterschiedlichem Ausmaß vorliegen.
Bei Patienten mit einseitiger Gesichtsdystrophie wird üblicherweise eine Asymmetrie der elektrischen Potentiale und der Hauttemperatur festgestellt, wobei die betroffene Seite überwiegt.
In den meisten Fällen kommt es zu einer Abnahme des oszillographischen Index und einem Krampf der Kapillaren auf der betroffenen Seite, was auf ein Überwiegen des Tonus des sympathischen Nervensystems hinweist.
Fast alle Patienten zeigen Veränderungen im Elektroenzephalogramm, die für eine Schädigung der hypothalamisch-mesenzephalen Formationen des Gehirns charakteristisch sind. Elektromyographische Untersuchungen zeigen fast immer Veränderungen der elektrischen Aktivität der Muskeln auf der Seite der Dystrophie, auch dort, wo klinisch atrophische Manifestationen im Gewebe beobachtet werden.
Basierend auf einer Reihe klinischer und physiologischer Forschungsdaten unterscheidet LA Shurinok zwei Stadien der Gesichtsatrophie: fortschreitend und stationär.
Diagnose fortschreitende Gesichtsatrophie
Die Hemiatrophie des Gesichts muss von der Asymmetrie bei angeborener (nicht-progressiver) Unterentwicklung des Gesichts, der Hemihypertrophie des Gesichts sowie dem muskulären Schiefhals, der fokalen Sklerodermie, der Gewebeatrophie bei Lipodystrophien und der Dermatomyositis unterschieden werden. Letztere Erkrankungen werden in Kursen zur allgemeinen Orthopädie und Dermatologie behandelt.
Behandlung fortschreitende Gesichtsatrophie
Chirurgische Behandlungsmethoden der progressiven Gesichtsatrophie sind erst (!) nach Unterbrechung oder Hemmung des Fortschreitens des Prozesses zulässig, d. h. in seinem zweiten abgeschlossenen Stadium. Zu diesem Zweck wird eine komplexe medikamentöse und physiotherapeutische Behandlung in Kombination mit einer vago-sympathischen Blockade und manchmal einer Blockade des zervikothorakalen Ganglions empfohlen.
Zur Verbesserung des Gewebestoffwechsels sollten Vitamine (Thiamin, Pyridoxin, Cyanocobalamin, Tocopherolacetat), Aloe, Glaskörper oder Lidase für 20–30 Tage verschrieben werden. Um den Stoffwechsel im Muskelgewebe anzuregen, wird 30 Tage lang 1–2 ml ATP intramuskulär verabreicht. Thiamin trägt zur Normalisierung des Kohlenhydratstoffwechsels bei, wodurch die Menge an ATP (gebildet durch oxidative Phosphorylierung in den Mitochondrien) zunimmt. Cyanocobalamin, Nerobol und Retabolil tragen zur Normalisierung des Proteinstoffwechsels bei.
Zur Beeinflussung der zentralen und peripheren Anteile des autonomen Nervensystems (ANS) werden Elektrophorese der zervikalen sympathischen Ganglien, ein galvanisches Halsband, endonasale Elektrophorese mit einer 2%igen Calciumchlorid- oder Diphenhydraminlösung (7-10 Sitzungen), UHF im Hypothalamusbereich (6-7 Sitzungen) und eine galvanische Halbmaske mit Lidase (Nr. 7-8) kombiniert.
Es ist notwendig, Reizquellen auszuschließen, die von der Leber, dem Magen, den Beckenorganen usw. ausgehen.
Bei erhöhtem Tonus des sympathischen und gleichzeitiger Schwäche der parasympathischen Teile des Nervensystems wird empfohlen, Sympatholytika und Cholinomimetika unter Berücksichtigung des Schadensniveaus zu kombinieren: Bei Schäden an den zentralen vegetativen Strukturen werden zentrale Adrenolytika verschrieben (Chlorpromazin, Oxazil, Reserpin usw.): Ganglien werden am besten mit Ganglioplegika (Pachycarpin, Hexonium, Pentamin, Gangleron usw.) behandelt. Wenn sowohl periphere als auch zentrale Teile des VNS an dem Prozess beteiligt sind, werden krampflösende Mittel wie Papaverin, Dibazol, Euphyllin, Platiphyllin, Khellin, Spasmolytin und Nikotinsäure verwendet.
Der sympathische Tonus wird durch die Begrenzung von Proteinen und Fetten in der Ernährung reduziert; zur Verstärkung des parasympathischen Effekts werden Acetylcholin, Carbachol sowie Anticholinesterase-Substanzen (z. B. Proserin, Oxamizin, Mestinon) und Antihistaminika (Diphenhydramin, Pipolfen, Suprastin) verschrieben. Darüber hinaus sind kohlenhydratreiche Lebensmittel, ein kühles Berg- oder Seeklima, Kohlendioxidbäder (37 °C) und andere von Neurologen verordnete Mittel und Methoden angezeigt (LA Shurinok, 1975).
Durch eine konservative präoperative Behandlung stabilisiert sich der Prozess, die Atrophie bleibt jedoch in der Regel äußerlich ausgeprägt.
Myogramme der Gesichtsmuskeln zeigen eine Zunahme ihrer bioelektrischen Aktivität, eine Abnahme oder sogar ein Verschwinden der Asymmetrie der Indikatoren für den Zustand des autonomen Nervensystems, in einer Reihe von Fällen (Anfangsformen der Erkrankung) eine Abnahme der Werte der elektrischen Potenziale der Gesichtshaut und das Verschwinden von Störungen in der Thermotopographie der Haut.
Methoden der chirurgischen Behandlung der progressiven Gesichtsatrophie
Zu den wichtigsten Methoden der chirurgischen Behandlung der Gesichtsatrophie gehören die folgenden.
- Paraffininjektionen unter die Haut der atrophierten Wange. Aufgrund von Thrombosen und Gefäßembolien wenden Chirurgen diese Methode derzeit nicht an.
- Subkutane Gewebetransplantation (aufgrund der allmählichen und ungleichmäßigen Faltenbildung hat sie ebenfalls keine breite Anwendung gefunden).
- Die Einführung von Kunststoff-Explantaten, die die Gesichtsasymmetrie im Ruhezustand beseitigen, gleichzeitig aber die betroffene Seite immobilisieren und die Symmetrie des Lächelns aufheben, ist für Patienten unzufrieden mit der Steifheit des Kunststoffs, der an typischerweise weichen und biegsamen Stellen eingesetzt wird. In dieser Hinsicht ist die Implantation poröser Kunststoffe erfolgversprechender, allerdings gibt es in der Literatur keine überzeugenden Berichte über die Ergebnisse ihrer Anwendung. Empfohlen wird auch die Verwendung von Silikon-Explantaten, die biologisch inert und stabil elastisch sind.
- Die Implantation der zerkleinerten Knorpel- und Bindegewebsbasis des Filatov-Schafts unter die Haut hat fast die gleichen Nachteile: Steifheit (Knorpel), die Fähigkeit, das Gesicht (Knorpel, Schaft) zu immobilisieren.
- Replantation eines deepidermisierten und subkutangewebefreien Hautlappens oder der Proteinhülle eines Stierhodens nach der Methode von Yu. I. Vernadsky.
Korrektur der Gesichtskonturen mit der Methode von Yu. I. Vernadsky
Im Unterkieferbereich wird ein Einschnitt vorgenommen, durch den die zuvor mit einer 0,25%igen Novocain-Lösung „angehobene“ Haut mit einer großen, gebogenen Cooper-Schere mit stumpfer Spitze oder einem speziellen Raspatorium mit langem Griff abgezogen wird.
Nachdem die entstandene Tasche von außen gestampft und gepresst wurde, werden die Konturen des zukünftigen Transplantates unter örtlicher Betäubung mit einer vorbereiteten Kunststoffschablone auf der Vorderseite des Bauches nachgezeichnet. Im markierten Bereich (vor der Transplantation) wird die Haut deepidermisiert und anschließend der Lappen abgetrennt, wobei darauf geachtet wird, das Unterhautgewebe nicht zu erfassen.
Nachdem der Lappen an Kunststofffäden (Haltern) befestigt wurde, werden deren Enden durch das Öhr von 3-4 geraden, dicken ("Zigeuner-") Nadeln gefädelt, mit deren Hilfe die Enden der Halter in die subkutane Wunde im Gesicht gezogen und dann aus den oberen und seitlichen Bögen der Wunde herausgeführt und an kleinen Jodoformrollen festgebunden werden. Auf diese Weise scheint das Hauttransplantat über die gesamte subkutane Wundoberfläche gespannt zu sein. Da das Transplantat auf beiden Seiten eine Wundoberfläche hat, wächst es in der Wundtasche mit der Haut und dem Unterhautgewebe zusammen.
An Stellen mit der größten Wangensenkung wird der Lappen verdoppelt oder in drei Schichten gelegt, indem eine Art "Patch"-Duplikat an den Hauptlappen genäht wird. Der kosmetische Effekt dieser Methode ist recht hoch: Gesichtsasymmetrie wird beseitigt; Die Beweglichkeit der betroffenen Gesichtshälfte ist zwar eingeschränkt, aber nicht vollständig gelähmt.
Während und nach der Operation treten normalerweise keine Komplikationen auf (es sei denn, es tritt eine Infektion auf, die zur Abstoßung des Transplantats oder Explantats führt). Mit der Zeit kommt es jedoch zu einer Atrophie der transplantierten Haut (oder anderen biologischen Materials), und eine neue Schicht muss hinzugefügt werden. Bei einigen Patienten entwickeln sich nach der Transplantation von deepidermisierter Autoskin allmählich größer werdende Talgzysten. In diesen Fällen wird empfohlen, die Haut über der Fettansammlung (an 2–3 Stellen) mit einer dicken Injektionsnadel zu punktieren und das Fett durch die Einstiche herauszudrücken. Anschließend wird die leere Höhle mit 95%igem Ethylalkohol gespült, um eine Denaturierung der aktivierten Talgdrüsenzellen zu bewirken; ein Teil des Alkohols wird 3–4 Tage lang unter einem Druckverband in der Höhle belassen.
Um die Bildung von Talgzysten (Atherome) und zusätzliche Traumata zu vermeiden, empfiehlt es sich, anstelle von Autoderma die Eiweißhülle eines Stierhodens zu verwenden, die mit einem Skalpell schachbrettartig perforiert und (analog zum Autoderma) unter die Haut der betroffenen Gesichtspartie gespritzt wird.
 [ 19 ]
[ 19 ]
Korrektur der Gesichtskontur mit der AT-Methode Titova und NI Yarchuk
Bei der Konturplastik wird die allogen konservierte breite Faszie des Oberschenkels verwendet. Sie wird ein- oder zweischichtig oder, wenn eine erhebliche Menge an Kunststoffmaterial erforderlich ist, ziehharmonikaförmig (gewellt) transplantiert.
Für 2,5–3 Wochen wird ein Druckverband im Gesicht angelegt.
2-3 Tage nach der Operation werden Schwankungen im Transplantationsbereich festgestellt, die nicht durch Flüssigkeitsansammlungen unter der Haut, sondern durch Schwellungen des Faszientransplantats und aseptische Entzündungen der Wunde verursacht werden.
Um die Schwellung nach der Operation zu reduzieren, wenden Sie drei Tage lang Kälte auf den Transplantationsbereich an und nehmen Sie fünf bis sieben Tage lang dreimal täglich 0,05 g Diphenhydramin oral ein.
Eine postoperative Transplantatschwellung ist gefährlich, wenn sich der Einschnitt zur Bildung des Bettes und zur Einführung der Faszie direkt über dem Transplantationsbereich befindet. Dies kann zu übermäßiger Spannung an den Wundrändern führen, wodurch diese sich trennen und ein Teil der Faszie herausfallen kann. Um diese Komplikation zu vermeiden, sollten die Hautschnitte außerhalb des Transplantationsbereichs liegen. Sollte dies dennoch auftreten, kann man sich im Frühstadium auf die Entfernung eines Teils des Faszientransplantats beschränken und die Wunde sekundär nähen.
Kommt es zu einer Infektion und einer Entzündung der Wunde, muss das gesamte Transplantat entfernt werden.
Trotz der starken Gewebeablösung bei der Faszientransplantation sind subkutane Hämatome und intradermale Blutungen äußerst selten, was teilweise durch die blutstillende Wirkung des Fasziengewebes erklärt werden kann. Das größte Risiko einer Hämatombildung besteht bei der Beseitigung ausgeprägter Deformationen der seitlichen Gesichtspartie. Eine starke Gewebeablösung durch einen Schnitt vor der Ohrmuschel schafft die Voraussetzung für eine Blutansammlung im unteren, geschlossenen Bereich des gebildeten Wundbetts. Bei Verdacht auf Hämatombildung empfiehlt es sich, einen Abfluss im unteren Wundbereich zu schaffen.
Komplikationen
Die schwerwiegendste Komplikation ist die Eiterung der Operationswunde, die auftritt, wenn sich das Transplantat oder das Empfängerbett infiziert. Um dies zu verhindern, müssen bei der Vorbereitung von Faszientransplantaten und während ihrer Transplantation die aseptischen Anforderungen strikt eingehalten werden. Dabei ist darauf zu achten, dass die Mundschleimhaut bei der Bildung des Bettes im Wangen- und Lippenbereich nicht beschädigt wird.
Das Auftreten einer Verbindung zwischen der Operationswunde und der Mundhöhle während der Operation ist eine Kontraindikation für die Transplantation von Faszien, Proteinmembranen usw. Ein erneuter Eingriff ist erst nach mehreren Monaten zulässig.
Unter Berücksichtigung der Tatsache, dass sich das subkutane Fettgewebe der menschlichen Fußsohle (mit einer Dicke von 5 bis 25 mm) sowie die Dermis des Fußes stark von dem Fett und der Dermis anderer Bereiche unterscheiden und dass sie sehr fest, dicht und elastisch sind und nur geringe antigene Eigenschaften aufweisen, empfehlen NE Sel'skiy et al. (1991) dieses Allomaterial für die Konturplastik des Gesichts. Nach der Anwendung bei 21 Patienten stellten die Autoren bei 3 Personen Eiterung und Abstoßung des Transplantats fest. Natürlich müssen die unmittelbaren und langfristigen Ergebnisse der Verwendung dieses plastischen Materials weiter untersucht werden, da die Fußsohlenhaut anders als die deepithelisierte Haut anderer Bereiche keine Schweiß- und Talgdrüsen aufweist, was (im Hinblick auf die Verhinderung der Zystenbildung) sehr wichtig ist.

