
Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Herzschmerz" verstehen - Studie findet Zusammenhang zwischen Stress und Herzversagen
Zuletzt überprüft: 02.07.2025
 ">
">Der Stress einer Herzinsuffizienz bleibt im Körper gespeichert und kann zu Rückfällen und anderen damit verbundenen Gesundheitsproblemen führen, wie eine Studie zeigt. Wissenschaftler haben herausgefunden, dass Herzinsuffizienz ein „Stressgedächtnis“ in Form von Veränderungen in der DNA hämatopoetischer Stammzellen hinterlässt, die an der Blutbildung beteiligt sind, sowie von Immunzellen, den sogenannten Makrophagen.
Diese Immunzellen spielen eine wichtige Rolle beim Schutz der Herzgesundheit. Allerdings wurde ein wichtiger Signalweg (eine Kette von Molekülen, die Signale innerhalb einer Zelle übertragen), der sogenannte Transformierende Wachstumsfaktor Beta (TGF-β), in hämatopoetischen Stammzellen bei Herzinsuffizienz unterdrückt, was sich negativ auf die Makrophagenproduktion auswirkte.
Durch die Verbesserung des TGF-β-Spiegels könnte eine neue Behandlungsmethode für wiederkehrende Herzinsuffizienz geschaffen werden, und durch die Erkennung einer Ansammlung von Stressgedächtnis könnte eine Frühwarnung erfolgen, bevor es zu einer solchen kommt.
Ein gesunder Lebensstil und ein verbessertes Wohlbefinden gehören zu den globalen Zielen für nachhaltige Entwicklung der UN. Eine aktuelle Studie zeigt, dass die Lebenserwartung weltweit bis 2050 um rund 4,5 Jahre steigen wird. Dies ist vor allem auf die Bemühungen des öffentlichen Gesundheitswesens zurückzuführen, Krankheiten vorzubeugen und die Überlebenschancen bei Erkrankungen wie Herz-Kreislauf-Erkrankungen zu verbessern. Dennoch sind Herzerkrankungen weltweit nach wie vor die häufigste Todesursache. Schätzungsweise 26 Millionen Menschen leiden an Herzinsuffizienz.
Ist eine Herzinsuffizienz erst einmal aufgetreten, kommt es häufig zu Rückfällen, begleitet von weiteren gesundheitlichen Problemen wie Nieren- und Muskelerkrankungen. Forscher in Japan wollten herausfinden, was diese Rückfälle und die Schädigung anderer Organe verursacht und ob sie verhindert werden können.
Die Studie wurde in der Fachzeitschrift Science Immunology veröffentlicht.
„Aufgrund unserer früheren Studien gingen wir davon aus, dass Rückfälle durch den Stress während einer Herzinsuffizienz verursacht werden könnten, der sich im Körper, insbesondere in den hämatopoetischen Stammzellen, ansammelt“, erklärte Projektprofessor Katsuito Fujio von der medizinischen Fakultät der Universität Tokio. Hämatopoietische Stammzellen befinden sich im Knochenmark und sind die Quelle von Blutzellen und Immunzellen, den sogenannten Makrophagen, die zum Schutz der Herzgesundheit beitragen.
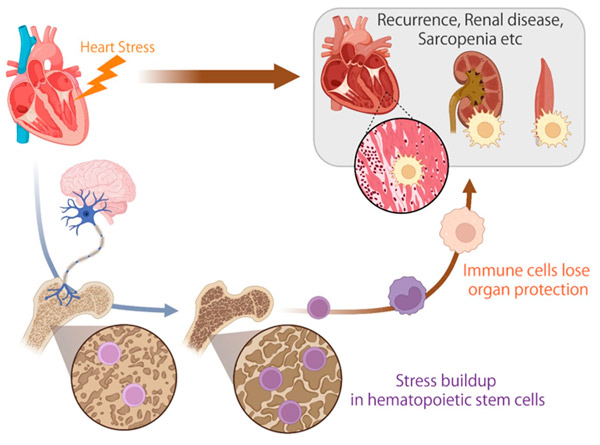
Diese Abbildung zeigt, dass bei Herzinsuffizienz Stresssignale an das Gehirn weitergeleitet werden, das sie dann über Nerven an hämatopoetische Stammzellen im Knochenmark weiterleitet, wo sie sich als Stressgedächtnis ansammeln. Diese stressakkumulierten Stammzellen produzieren Immunzellen mit verminderter Schutzfunktion für Organe wie Herz, Nieren und Muskeln. Quelle: Science Immunology (2024). DOI: 10.1126/sciimmunol.ade3814
Bei Mäusen mit Herzinsuffizienz fanden die Forscher Hinweise auf Stress-Imprinting im Epigenom, d. h. chemische Veränderungen in der DNA der Mäuse. Ein wichtiger Signalweg namens Transforming Growth Factor Beta, der an der Regulierung vieler zellulärer Prozesse beteiligt ist, wurde in den hämatopoetischen Stammzellen der Mäuse mit Herzinsuffizienz unterdrückt, was zur Produktion dysfunktionaler Immunzellen führte.
Diese Veränderungen blieben über die Zeit bestehen. Als das Team Knochenmark von Mäusen mit Herzinsuffizienz in gesunde Mäuse transplantierte, stellte es fest, dass die Stammzellen weiterhin dysfunktionale Immunzellen produzierten. Diese Mäuse entwickelten daraufhin eine Herzinsuffizienz und wurden anfällig für Organschäden.
„Wir haben dieses Phänomen als Stressgedächtnis bezeichnet, da der Stress einer Herzinsuffizienz lange in Erinnerung bleibt und den gesamten Körper weiterhin beeinflusst. Obwohl auch verschiedene andere Arten von Stress dieses Stressgedächtnis hinterlassen können, glauben wir, dass der durch eine Herzinsuffizienz verursachte Stress besonders bedeutsam ist“, sagte Fujio.
Die gute Nachricht ist, dass die Identifizierung und das Verständnis dieser Veränderungen im TGF-β-Signalweg neue Möglichkeiten für potenzielle zukünftige Behandlungen eröffnen.
„Völlig neue Therapien könnten in Betracht gezogen werden, um die Ansammlung dieses Stressgedächtnisses während eines Krankenhausaufenthalts bei Herzinsuffizienz zu verhindern“, sagte Fujio. „Bei Tieren mit Herzinsuffizienz hat sich die Gabe von zusätzlichem aktivem TGF-β als potenzielle Behandlungsoption erwiesen. Die Korrektur des Epigenoms hämatopoetischer Stammzellen könnte ebenfalls ein Weg sein, das Stressgedächtnis zu beseitigen.“
Nachdem dies nun erkannt wurde, hofft das Team, ein System entwickeln zu können, das die Ansammlung von Stressgedächtnis bei Menschen erkennen und verhindern kann. Langfristig soll damit nicht nur ein erneutes Auftreten von Herzversagen verhindert, sondern auch die Krankheit erkannt werden, bevor sie sich voll entwickelt.
