
Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Arteriovenöse Malformation
Facharzt des Artikels
Zuletzt überprüft: 04.07.2025
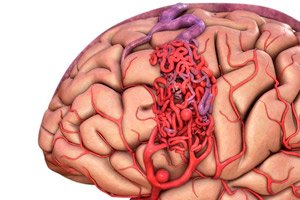
Die arteriovenöse Malformation ist ein angeborener Defekt in der Entwicklung von Blutgefäßen, der durch das Vorhandensein eines abnormalen Netzwerks arteriovenöser Anastomosen gekennzeichnet ist. Am häufigsten befinden sich arteriovenöse Malformationen in der hinteren Schädelgrube und haben eine recht typische Struktur – eine oder zwei echte Arterien, ein Gewirr von AVMs und eine drainierende Vene.
 [ 1 ]
[ 1 ]
Ursachen arteriovenöse Malformation
Die Ursachen für die Entstehung einer AVM sind noch nicht vollständig geklärt, es wird jedoch vermutet, dass genetische und umweltbedingte Faktoren eine Rolle spielen. Hier sind einige mögliche Ursachen für die Entstehung einer AVM:
- Genetische Faktoren: Studien haben gezeigt, dass bei manchen Patienten mit AVM die Erkrankung in der Familie vorkommt. Genetische Mutationen können bei der Entstehung der Gefäßanomalie eine Rolle spielen.
- Angeborene Defekte: Angeborene Gefäßanomalien können sich während der Embryonalentwicklung entwickeln. Diese können auf Fehler bei der Entwicklung des Gefäßgewebes des Gehirns zurückzuführen sein.
- Umweltfaktoren: Einige Studien haben einen Zusammenhang zwischen AVM und bestimmten Umweltfaktoren wie Strahlung oder toxischer Belastung während der Schwangerschaft gezeigt. Diese Zusammenhänge sind jedoch nicht immer bestätigt und erklären nicht alle Fälle von AVM.
- Regionale Faktoren: In einigen Fällen kann AVM mit bestimmten geografischen Gebieten oder ethnischen Gruppen in Verbindung gebracht werden, aber diese Zusammenhänge erfordern weitere Untersuchungen.
Neben diesen Faktoren, die die Entstehung einer AVM beeinflussen können, ist es wichtig zu beachten, dass es sich um eine angeborene Erkrankung handelt, die in der Regel bei der Geburt oder in der frühen Kindheit festgestellt wird, obwohl Symptome auch später im Leben auftreten können. Weitere Forschung ist erforderlich, um die Ursachen und Mechanismen der AVM-Entwicklung genau zu verstehen.
Pathogenese
Am gefährlichsten ist der Riss der Malformationswände, der mit einer spontanen intrakraniellen Blutung einhergeht. Dies geschieht, weil in den Malformationsgefäßen unter Druck nahe dem arteriellen Blut zirkuliert. Und natürlich führt hoher Druck zur Dehnung der degenerativ veränderten Gefäße, einer Vergrößerung ihres Volumens und einer Ausdünnung der Gefäßwände. Schließlich tritt der Riss an der dünnsten Stelle auf. Laut Statistik passiert dies bei 42–60 % der Patienten mit AVM. Die Sterblichkeit bei der ersten AVM-Ruptur beträgt 12–15 %. Bei den übrigen kann die Blutung ohne Periodizität erneut auftreten. Wir beobachteten einen Patienten, der im Laufe von 8 Jahren elf spontane intrakraniale Blutungen hatte. Dieser relativ „gutartige“ Verlauf einer AVM-Ruptur im Vergleich zur Ruptur arterieller Aneurysmen erklärt sich durch die Besonderheiten der hämodynamischen Störungen, die nach der Ruptur auftreten. Es ist bekannt, dass der Riss eines arteriellen Aneurysmas am häufigsten zu einer Subarachnoidalblutung (SAB) und der Entwicklung eines Angiospasmus führt, der in den ersten Minuten einen schützenden Charakter hat und dabei hilft, die Blutung schnell zu stoppen, später jedoch eine große Gefahr für das Leben des Patienten darstellt.
Es ist der Angiospasmus, der zu zerebraler Ischämie und Ödemen führt und den Schweregrad des Zustands des Patienten und die Prognose bestimmt. Im Gegensatz dazu verbessert ein Angiospasmus der afferenten Arterien der AVM die Blutversorgung des Gehirns aufgrund einer Verringerung des arteriovenösen Ausflusses. Wenn eine AVM reißt, bilden sich häufiger intrazerebrale und subdurale Hämatome. Der Durchbruch von Blut in die Subarachnoidalzisternen ist sekundär. Blutungen aus der gerissenen Wand der AVM stoppen schneller, da der Blutdruck darin niedriger ist als in den Hauptarterien und die Wand anfälliger für eine Kompression durch das austretende Blut ist. Natürlich endet dies nicht immer gut für den Patienten. Die gefährlichsten AVM-Rupturen befinden sich in der Nähe der Hirnventrikel, in den subkortikalen Ganglien und im Hirnstamm. In dieser Situation hilft ein Angiospasmus der zuführenden Arterien, die Blutung zu stoppen.
Der entscheidende Faktor in der Pathogenese einer AVM-Ruptur ist die Menge des ausgetretenen Blutes und die Lokalisation des Hämatoms. Hemisphärische intrazerebrale Hämatome verlaufen selbst bei einem Volumen von bis zu 60 cm 3 relativ günstig. Sie können schwere fokale neurologische Störungen verursachen, führen aber selten zu schweren lebensbedrohlichen Erkrankungen. Eine Hämatomruptur in die Hirnventrikel verschlechtert die Prognose deutlich. Einerseits erhöht Blut, das das Ependym der Ventrikel reizt, die Produktion von Liquor cerebrospinalis, andererseits führt die Beeinträchtigung des Ventrikelbodens zu schweren Funktionsstörungen der lebenswichtigen Zentren im Hypothalamus. Die Ausbreitung des Blutes im gesamten Ventrikelsystem führt zu dessen Tamponade, die an sich nicht mit dem Leben vereinbar ist.
In die Subarachnoidalzisternen eingedrungenes Blut stört zudem die Liquorzirkulation und erschwert den Zugang der Liquorflüssigkeit zu den blutgestauten Pacchion-Granulationen. Infolgedessen verlangsamt sich die Resorption der Liquorflüssigkeit, und es kann sich eine akute Liquorhypertonie entwickeln, gefolgt von einem inneren und äußeren Hydrozephalus. Durch den Abbau der gebildeten Bestandteile des ausgetretenen Blutes entstehen zahlreiche toxische Substanzen, die meist vasoaktiv wirken. Dies führt einerseits zu einer Vasokonstriktion der kleinen Pialarterien, andererseits zu einer erhöhten Kapillardurchlässigkeit. Blutabbauprodukte beeinflussen zudem Nervenzellen, verändern deren biochemische Prozesse und stören die Durchlässigkeit der Zellmembranen. Zunächst verändert sich die Funktion der Kalium-Natrium-Pumpe, Kalium beginnt die Zelle zu verlassen, und das Natriumkation, das viermal hydrophiler als Kalium ist, tritt an seine Stelle.
Dies führt zunächst zu einem intrazellulären Ödem im Bereich der Blutung und dann zu einer Schwellung der Zellen. Hypoxie trägt ebenfalls zur Entstehung von Ödemen bei, die aufgrund der Kompression der Hirngefäße durch das Hämatom und des bereits erwähnten erhöhten Liquordrucks unvermeidlich sind. Eine Funktionsstörung der dienzephalen Teile des Gehirns und vor allem die Regulierung des Wasser-Elektrolyt-Haushalts führen zu Flüssigkeitsansammlungen im Körper und Kaliumverlust, was ebenfalls die ödematöse Reaktion des Gehirns verstärkt. Die Pathogenese einer AVM-Ruptur ist nicht auf zerebrale Erkrankungen beschränkt. Nicht weniger gefährlich sind extrazerebrale Komplikationen. Dies ist in erster Linie das zerebrokardiale Syndrom, das im Elektrokardiogramm eine akute Koronarinsuffizienz vortäuschen kann.
Patienten mit intrazerebralen Blutungen entwickeln relativ schnell eine Lungenentzündung und Atemversagen. Die Bakterienflora spielt dabei eine untergeordnete Rolle. Der primäre Effekt ist der zentrale Einfluss auf die Lunge, bestehend aus ausgedehntem Bronchospasmus, erhöhter Auswurf- und Schleimproduktion, Ischämie des Lungenparenchyms durch ausgedehnten Krampf der kleinen Lungenarterien, was schnell zu dystrophischen Erkrankungen, Abschuppung des Alveolarepithels und einer Abnahme der Gasaustauschfunktion der Lunge führt.
Wenn dies mit einer Unterdrückung des Hustenreflexes, einem bulbären Atemversagen, einhergeht, besteht eine ernsthafte Bedrohung für das Leben des Patienten. In den meisten Fällen ist die darauf folgende eitrige Trachyobronchitis schlecht auf eine antibakterielle Therapie ansprechbar und verschlimmert das Atemversagen, was sich unmittelbar auf die Zunahme der zerebralen Hypoxie auswirkt. Somit kann die Verletzung der äußeren Atmung, selbst bei relativer Kompensation zerebraler Störungen, zum Tod führen. Oft erlangen Patienten nach einem Koma das Bewusstsein wieder, sterben dann aber an zunehmendem Atemversagen und hypoxischem Hirnödem.
Dystrophische Veränderungen entwickeln sich schnell nicht nur in der Lunge, sondern auch in Leber, Magen-Darm-Trakt, Nebennieren und Nieren. Harnwegsinfektionen und Dekubitus, die sich ohne gute Patientenversorgung schnell entwickeln, stellen eine Gefahr für das Leben des Patienten dar. Diese Komplikationen können jedoch vermieden werden, wenn Ärzte sie im Auge behalten und wissen, wie sie ihnen entgegenwirken können.
Zusammenfassend lässt sich sagen, dass die Mortalität bei solchen intrakraniellen Blutungen niedriger ist als bei arteriellen Aneurysmen und hypertensiven hämorrhagischen Schlaganfällen, obwohl sie 12-15 % erreicht. AVMs sind durch wiederholte, manchmal multiple Blutungen mit unterschiedlicher, unmöglich vorherzusagender Häufigkeit gekennzeichnet. Bei einem ungünstigen Verlauf der posthämorrhagischen Phase können die aufgeführten pathogenetischen Mechanismen zum Tod führen.
Symptome arteriovenöse Malformation
Hämorrhagischer Krankheitstyp (50-70% der Fälle). Dieser Typ ist gekennzeichnet durch das Vorhandensein einer arteriellen Hypertonie beim Patienten, eine geringe Größe des Fehlbildungsknotens, seine Drainage in tiefe Venen und eine arteriovenöse Fehlbildung der hinteren Schädelgrube.
Der hämorrhagische Typ ist in 50 % der Fälle das erste Symptom der Manifestation einer arteriovenösen Malformation, verursacht detaillierte Ergebnisse bei 10 – 15 % und Behinderungen bei 20 – 30 % der Patienten (N. Martin et al.). Das jährliche Blutungsrisiko bei Patienten mit arteriovenöser Malformation beträgt 1,5 – 3 %. Das Risiko erneuter Blutungen während des ersten Jahres beträgt 8 % und steigt mit dem Alter an. Blutungen aus arteriovenöser Malformation sind die Ursache für 5 – 12 % aller Müttersterblichkeit und 23 % aller intrakraniellen Blutungen bei schwangeren Frauen. Das Bild einer Subarachnoidalblutung wird bei 52 % der Patienten beobachtet. Bei 17 % der Patienten treten komplizierte Formen von Blutungen auf: Bildung von intrazerebralen (38 %), subduralen (2 %) und gemischten (13 %) Hämatomen, bei 47 % entwickelt sich eine Hämotamponade der Ventrikel.
Der torpide Verlauf ist typisch für Patienten mit großen arteriovenösen Malformationen im Kortex. Die Blutversorgung der arteriovenösen Malformation erfolgt über Äste der mittleren Hirnarterie.
Die charakteristischsten Symptome des torpiden Verlaufs sind das Krampfsyndrom (bei 26–27 % der Patienten mit arteriovenöser Malformation), Cluster-Kopfschmerzen und fortschreitende neurologische Defizite, wie bei Hirntumoren.
Varianten der klinischen Manifestationen arteriovenöser Missbildungen
Wie bereits erwähnt, ist die häufigste klinische Erstmanifestation einer AVM eine spontane intrakraniale Blutung (40–60 % der Patienten). Sie tritt oft ohne Vorwarnung und bei völliger Gesundheit auf. Auslöser können körperliche Anstrengung, Stresssituationen, neuropsychische Anspannung, hohe Alkoholmengen usw. sein. Im Moment der AVM-Ruptur verspüren die Patienten einen plötzlichen, stechenden Kopfschmerz, der wie ein Schlag oder eine Ruptur wirkt. Die Schmerzen nehmen schnell zu und verursachen Schwindel, Übelkeit und Erbrechen.

Der Bewusstseinsverlust kann innerhalb weniger Minuten eintreten. In seltenen Fällen können die Kopfschmerzen leicht sein, die Patienten verlieren nicht das Bewusstsein, spüren aber eine Schwächung und Taubheit ihrer Gliedmaßen (meist kontralateral zur Blutung) und sind sprachbehindert. In 15 % der Fälle manifestiert sich die Blutung als voll ausgeprägter epileptischer Anfall, nach dem die Patienten komatös bleiben können.
Zur Bestimmung des Schweregrads einer AVM-Blutung kann die oben angegebene Hunt-Hess-Skala mit einigen Anpassungen als Grundlage verwendet werden. Da AVM-Blutungen sehr unterschiedliche Symptome aufweisen können, können fokale neurologische Symptome allgemeine zerebrale Symptome überwiegen. Daher können Patienten mit Bewusstseinsstufen auf Stufe I oder II der Skala schwere fokale neurologische Störungen (Hemiparese, Hemihypästhesie, Aphasie, Hemianopsie) aufweisen. Im Gegensatz zu aneurysmatischen Blutungen wird die AVM-Ruptur nicht durch den Schweregrad und die Prävalenz des Angiospasmus bestimmt, sondern durch das Volumen und die Lokalisation des intrazerebralen Hämatoms.
Das Meningealsyndrom entwickelt sich nach mehreren Stunden und kann unterschiedlich stark ausgeprägt sein. Der Blutdruck steigt in der Regel an, jedoch nicht so stark und nicht so lange wie bei rupturierten arteriellen Aneurysmen. Normalerweise überschreitet dieser Anstieg 30–40 mmHg nicht. Am zweiten oder dritten Tag tritt eine Hyperthermie zentraler Genese auf. Der Zustand der Patienten verschlechtert sich natürlicherweise mit zunehmendem Hirnödem und verstärktem Abbau des verschütteten Blutes. Dies hält bis zu 4–5 Tage an. Bei günstigem Verlauf beginnt sich der Zustand der Patienten nach Stabilisierung am 6.–8. Tag zu verbessern. Die Dynamik der Herdsymptome hängt von der Lokalisation und Größe des Hämatoms ab.
Bei Blutungen in funktionell wichtigen Hirnarealen oder bei der Zerstörung motorischer Leiter treten sofort Ausfallsymptome auf, die lange Zeit ohne Dynamik anhalten. Treten die Ausfallsymptome nicht sofort auf, sondern verstärken sich parallel zum Hirnödem, ist mit einer Wiederherstellung des Defizits nach 2-3 Wochen zu rechnen, wenn das Ödem vollständig zurückgeht.
Das klinische Bild einer AVM-Ruptur ist sehr vielfältig und hängt von vielen Faktoren ab. Die wichtigsten sind: das Volumen und der Ort der Blutung, die Schwere der Hirnödemreaktion und der Grad der Beteiligung der Hirnstammstrukturen am Prozess.
Arteriovenöse Malformationen können sich in epileptiformen Anfällen äußern (30–40 %). Ursache für ihre Entwicklung können Blutkreislaufstörungen in benachbarten Hirnarealen aufgrund des Steal-Phänomens sein. Darüber hinaus kann die Malformation selbst die Großhirnrinde reizen und epileptische Entladungen auslösen. Wir haben bereits über bestimmte Arten von AVM gesprochen, um die sich eine Gliose des Hirngewebes entwickelt, die sich ebenfalls häufig in epileptischen Anfällen äußert.
Ein durch eine AVM verursachtes epileptisches Syndrom ist dadurch gekennzeichnet, dass es im Erwachsenenalter ursachenlos auftritt, oft ohne auslösenden Faktor. Anfälle können generalisiert oder fokal sein. Das Vorhandensein einer klaren fokalen Komponente bei einem epileptischen Anfall ohne allgemeine zerebrale Symptome sollte den Gedanken an eine mögliche AVM wecken. Selbst generalisierte Anfälle, die mit Krämpfen hauptsächlich derselben Gliedmaßen und einer erzwungenen Drehung von Kopf und Augen zur einen oder anderen Seite beginnen, sind oft Ausdruck einer AVM. Seltener erleben Patienten leichte Anfälle wie Absencen oder Dämmerzustand. Häufigkeit und Periodizität epileptischer Anfälle können variieren und von isoliert bis wiederkehrend reichen.
Formen
VV Lebedev und Co-Autoren identifizierten anhand von EKG-Daten drei Varianten des zerebrokardialen Syndroms:
- Typ I - Verletzung der Funktionen des Automatismus und der Erregbarkeit (Sinustachykardie oder Bradykardie, Arrhythmie, Vorhofflimmern);
- Typ II – Veränderungen der Repolarisationsprozesse, vorübergehende Veränderungen in der Endphase des Ventrikelkomplexes je nach Ischämietyp, Myokardschädigung mit Veränderungen der T-Welle und der Position des ST-Segments;
- Typ III – Reizleitungsstörung (Blockade, Anzeichen einer erhöhten Belastung des rechten Herzens). Diese EKG-Veränderungen können kombiniert werden und ihr Schweregrad korreliert mit dem Schweregrad des Allgemeinzustandes der Patienten.
Komplikationen und Konsequenzen
Eine arteriovenöse Malformation (AVM) ist eine angeborene Gefäßanomalie, bei der Arterien und Venen ohne dazwischenliegende Kapillarschicht miteinander verbunden sind. Komplikationen und Folgen von AVMs können schwerwiegend sein und hängen von Größe, Lage und Merkmalen der jeweiligen Malformation ab. Dazu gehören unter anderem:
- Schlaganfall: Eine der schwerwiegendsten Komplikationen von AVM ist das Schlaganfallrisiko. Fehlbildungen können zu abnormalen Blutflusswegen führen, die zu Hirnblutungen und damit zu einem Schlaganfall führen können. Schlaganfälle können unterschiedlich schwerwiegend sein und bleibende neurologische Defizite hinterlassen.
- Epilepsie: AVMs können bei manchen Patienten epileptische Anfälle auslösen, insbesondere wenn sich die Fehlbildung in bestimmten Bereichen des Gehirns befindet.
- Blutung: Fehlbildungen können unvorhersehbar sein und zu Hirnblutungen führen. Dies kann eine lebensbedrohliche Komplikation sein und schwerwiegende Folgen haben.
- Hydrozephalus: Wenn sich die AVM in der Nähe der Hirnventrikel befindet, kann sie einen Hydrozephalus verursachen, der zur Ansammlung von zusätzlicher Flüssigkeit im Gehirn und zu erhöhtem Hirndruck führen kann.
- Neurologische Defizite: Eine AVM kann das umliegende Hirngewebe schädigen und verschiedene neurologische Defizite verursachen, darunter Lähmungen, sensorische Störungen und Defizite bei der Sprach- und Motorikkoordination.
- Schmerzen und Kopfschmerzen: Bei Patienten mit AVM können aufgrund der Fehlbildung chronische Schmerzen und Kopfschmerzen auftreten.
- Psychische Auswirkungen: Komplikationen durch AVM können erhebliche Auswirkungen auf das psychische Wohlbefinden der Patienten haben und zu Angstzuständen, Depressionen und Stress führen.
- Einschränkungen des Lebensstils: Sobald eine AVM erkannt wird, benötigen die Patienten möglicherweise Änderungen ihres Lebensstils und Empfehlungen zum Risikomanagement, einschließlich der Einschränkung körperlicher Aktivität und bestimmter Aktivitäten.
Diagnose arteriovenöse Malformation
Die Diagnose einer arteriovenösen Malformation (AVM) umfasst typischerweise verschiedene bildgebende Verfahren, um das Vorhandensein der Malformation zu bestätigen und ihre Merkmale zu beurteilen. Die wichtigsten Methoden zur Diagnose einer AVM sind:
- Magnetresonanzangiographie (MRA): Die MRA ist eine der wichtigsten Methoden zur Diagnose von AVM. Es handelt sich um eine nicht-invasive Untersuchung, die die Struktur der Blutgefäße und den Blutfluss im Gehirn mithilfe von Magnetfeldern und Radiowellen visualisiert. Mithilfe der MRA können Lage, Größe und Form der AVM bestimmt werden.
- Digitale Subtraktionsangiographie (DSA): Dies ist ein invasiveres Verfahren, bei dem ein Kontrastmittel über einen Katheter direkt in die Gefäße injiziert wird und Röntgenstrahlen verwendet werden, um qualitativ hochwertige Bilder der Hirngefäße zu erzeugen. Die DSA ermöglicht eine detailliertere Untersuchung der AVM-Struktur und der Blutflussmuster.
- Computertomographie (CT): Mithilfe der CT können AVM erkannt und mögliche Komplikationen wie Blutungen beurteilt werden. Bei Bedarf kann ein Kontrastmittel zur besseren Darstellung eingesetzt werden.
- Gefäßduplex-Scan (Duplex-Ultraschall): Diese Technik kann nützlich sein, um die Gefäße im Hals- und Kopfbereich zu untersuchen und mit AVM verbundene Durchblutungsstörungen zu identifizieren.
- Magnetresonanzspektroskopie (MRS): MRS kann Informationen über die chemische Zusammensetzung des Gewebes im Bereich der AVM liefern und Anzeichen von Stoffwechselveränderungen aufdecken.
- Echoenzephalographie: Dies ist eine Ultraschalluntersuchung, mit der der Blutfluss und die Gehirnstruktur beurteilt werden können.
- Computertomographie-Angiographie (CTA): Die CTA kombiniert CT und Angiographie, um dreidimensionale Bilder der Blutgefäße im Gehirn zu erzeugen.
Sobald eine AVM diagnostiziert wurde, ist eine detaillierte Beurteilung der Merkmale der Fehlbildung, wie Größe, Form und Schweregrad, wichtig. Dies hilft zu bestimmen, ob eine Behandlung erforderlich ist und welche Behandlungsoption am besten geeignet ist, darunter chirurgische Entfernung, Embolisation, Strahlentherapie oder Beobachtung. Die Entscheidung zur Behandlung einer AVM sollte gemeinsam zwischen Patient und medizinischem Team unter Berücksichtigung der individuellen Umstände des Einzelfalls getroffen werden.
Differenzialdiagnose
Die Differentialdiagnose arteriovenöser Malformationen (AVM) kann ein wichtiger Schritt bei der Beurteilung von Patienten mit Gefäßveränderungen im Gehirn sein. AVM sind Gefäßanomalien, bei denen Arterien und Venen ohne dazwischenliegende Kapillarschicht miteinander verbunden sind. Sie können eine Vielzahl von Symptomen und Erkrankungen verursachen, und die Abgrenzung zu anderen Gefäßerkrankungen ist für eine angemessene Behandlung wichtig. Einige Erkrankungen, die eine Differentialdiagnose mit AVM erfordern können, sind:
- Schlaganfall: Schlaganfälle können die Symptome einer AVM imitieren, insbesondere wenn der Schlaganfall durch Gefäßveränderungen verursacht wird. Zur Unterscheidung kann eine Computertomographie (CT) oder Magnetresonanztomographie (MRT) des Gehirns erforderlich sein, um die Gefäßveränderungen sichtbar zu machen.
- Hämatom: Hämatome, wie z. B. ein subdurales oder epidurales Hämatom, können AVM-Symptome imitieren, insbesondere wenn sie von Kopfschmerzen und neurologischen Symptomen begleitet werden. Eine CT- oder MRT-Untersuchung kann helfen, die Ursache der Symptome zu ermitteln.
- Hirntumore: Hirntumore können verschiedene Symptome verursachen, die denen einer arteriellen vaskulären Venenthrombose ähneln können. Die Diagnose kann eine MRT mit Kontrastmittel und andere bildgebende Verfahren umfassen.
- Migräne: Migräne mit Aura kann AVM-Symptome wie Sehstörungen und Schwindel imitieren. Anamnese und zusätzliche Tests können helfen, die beiden Symptome zu unterscheiden.
- Zerebrale Vaskulitis: Eine Vaskulitis kann zu Entzündungen der Blutgefäße und Gefäßanomalien führen, die den Symptomen einer AVM ähneln können. Zur Diagnose einer Vaskulitis kann eine Biopsie oder Angiographie eingesetzt werden.
- Venenthrombose: Venenthrombosen können die Symptome einer AVM imitieren, insbesondere wenn der venöse Abfluss aus dem Gehirn gestört ist. Zusätzliche Untersuchungen können bei der Identifizierung einer Thrombose helfen.
Zur genauen Differentialdiagnose von AVM umfasst die Untersuchung eine umfassende klinische Untersuchung, neuroedukative Methoden (CT, MRT, Angiographie), manchmal eine Biopsie und andere spezialisierte Verfahren, abhängig von den spezifischen Symptomen und Umständen.
Wen kann ich kontaktieren?
Behandlung arteriovenöse Malformation
Die Behandlung einer arteriovenösen Malformation (AVM) hängt von ihrer Größe, ihrem Ort, ihren Symptomen und möglichen Komplikationen ab. In manchen Fällen kann eine AVM klein und asymptomatisch sein und erfordert keine aktive Behandlung. Bei Symptomen oder Blutungsgefahr kann jedoch eine Behandlung erforderlich sein. Zu den Behandlungsmöglichkeiten für AVM gehören:
- Operation: Die chirurgische Entfernung der AVM kann in Fällen erwogen werden, in denen die Fehlbildung an einer gut erreichbaren Stelle liegt und von geringer Komplexität ist. Die chirurgische Entfernung kann dazu beitragen, das Blutungsrisiko zu verringern und die Symptome zu lindern. Es handelt sich um einen komplexen Eingriff, der Risiken wie Schäden an umliegendem Gewebe und Nerven birgt.
Offene (transkranielle) Interventionen:
- Stadium I – Koagulation der Afferenzen;
- Stadium II – Isolierung des Kerns der arteriovenösen Malformation;
- Stadium III – Ligatur und Koagulation des Abflusses und Entfernung der arteriovenösen Malformation,
Endovaskuläre Eingriffe:
- stationärer Ballonverschluss der zuführenden Arterien – In-Flow-Embolisation (unkontrolliert);
- Kombination aus temporärer oder permanenter Ballonokklusion mit In-Flow-Embolisation;
- superselektive Embolisation.
Arteriovenöse Malformationen werden auch mit Radiochirurgie (Gamma-Knife, Cyber-Knife, Li-Nac usw.) behandelt.
- Embolisation: Bei der Embolisation werden medizinische Materialien oder Klebstoffe in die Blutgefäße eingebracht, um den Blutfluss zur AVM zu blockieren. Die Embolisation kann als vorbereitende Maßnahme vor einer Operation oder als eigenständige Behandlung eingesetzt werden. Sie kann dazu beitragen, Blutungen zu reduzieren und die Größe der AVM zu verringern.
- Strahlentherapie: Strahlentherapie kann zur Behandlung von AVMs eingesetzt werden, insbesondere in Fällen, in denen andere Behandlungen zu riskant sind. Die Strahlentherapie zielt darauf ab, die Blutung der AVM zu reduzieren und kann mehrere Sitzungen erfordern.
- Medikamente: In manchen Fällen können Medikamente eingesetzt werden, um Symptome wie Schmerzen oder Krämpfe zu lindern. Medikamente können auch zur Blutdruckkontrolle eingesetzt werden, um das Blutungsrisiko zu senken.
- Beobachtung und Symptombehandlung: In manchen Situationen, insbesondere wenn die AVM klein ist und keine Symptome verursacht, kann entschieden werden, den Zustand einfach zu beobachten und die Symptome nach Bedarf zu behandeln.
Die Behandlung von AVM muss für jeden Patienten individuell erfolgen, und die Wahl der Methode hängt von den spezifischen Umständen ab. Es ist wichtig, alle Behandlungsmöglichkeiten mit einem Arzt zu besprechen und den Patienten gründlich zu untersuchen, um den besten Behandlungsplan festzulegen. Die Behandlung kann erfolgreich sein, und Patienten können eine Besserung oder vollständige Genesung erreichen, aber jeder Fall ist einzigartig.
Prognose
Die Prognose einer arteriovenösen Malformation (AVM) hängt von verschiedenen Faktoren ab, darunter Größe, Lokalisation, Symptome, Patientenalter und Behandlungserfolg. Es ist wichtig zu bedenken, dass eine AVM eine Erkrankung ist, die sich bei verschiedenen Patienten unterschiedlich darstellen kann und deren Prognose von Person zu Person unterschiedlich ausfallen kann. Hier sind einige allgemeine Aspekte der Prognose einer AVM:
- Blutungsrisiko: Das Hauptrisiko einer AVM ist das Risiko einer Blutung (Blutung) im Gehirn. Kleine AVM mit geringem Blutungsrisiko haben möglicherweise eine gute Prognose und verursachen keine ernsthaften Probleme. Große und mittelgroße AVM können jedoch ein erhebliches Risiko darstellen.
- Symptome: Symptome einer AVM wie Kopfschmerzen, Krampfanfälle, Lähmungen oder Gefühlsstörungen können die Prognose beeinflussen. In einigen Fällen kann eine erfolgreiche Behandlung die Symptome lindern oder beseitigen.
- Größe und Lage: AVMs an gefährlicheren Stellen, z. B. tief im Gehirn oder in der Nähe kritischer Strukturen, haben möglicherweise eine schlechtere Prognose. Allerdings können auch viele große AVMs erfolgreich behandelt werden.
- Behandlung: Die Behandlung von AVMs kann die chirurgische Entfernung, Embolisation, Strahlentherapie oder Medikamente umfassen. Eine erfolgreiche Behandlung kann das Blutungsrisiko verringern und die Prognose verbessern.
- Alter: Auch das Alter des Patienten kann die Prognose beeinflussen. Kinder und junge Erwachsene haben oft eine bessere Prognose als ältere Patienten.
- Komorbiditäten: Das Vorhandensein anderer Erkrankungen oder Risikofaktoren wie Bluthochdruck oder Blutgerinnungsstörungen kann die Prognose und Behandlung von AVM beeinflussen.
Es ist wichtig zu beachten, dass AVM eine sorgfältige medizinische Überwachung und Behandlung erfordert. Die Entscheidung über die Behandlungsmethode und die Prognose sollte von qualifizierten Neurochirurgen und Neuroradiologen auf der Grundlage einer umfassenden Beurteilung jedes Einzelfalls getroffen werden.

