
Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Klassifizierung von Brustkrebs
Facharzt des Artikels
Zuletzt überprüft: 04.07.2025
Die Vielfalt der morphologischen Merkmale, der klinischen Manifestationen und der Reaktionen auf therapeutische Effekte geben allen Grund, Brustkrebs als heterogene Erkrankung zu definieren. Daher gibt es heute nicht nur eine, sondern mehrere Klassifikationen von Brustkrebs. Und jede von ihnen basiert auf ihren eigenen Prinzipien.
TNM-Klassifikation des Brustkrebses
Die Stadien von Brustkrebs werden durch die TNM-Klassifikation bösartiger Tumoren bestimmt, die von der WHO für alle bösartigen Neubildungen übernommen wurde. Für die onkologische Mammologie wurde sie basierend auf den Empfehlungen führender Spezialisten mit der Einführung von Details angepasst.
Die TNM-Klassifikation von Brustkrebs misst den anatomischen Grad des Tumors anhand seiner Größe, der Ausbreitung auf Lymphknoten in Achselhöhlen, Hals und Brust sowie dem Vorhandensein von Metastasen. Diese internationale Klassifikation von Brustkrebs wird von der International Association for Breast Cancer und der European Society for Medical Oncology (EUSOMA) übernommen.
Gemäß der TNM-Klassifikation verläuft Brustkrebs in folgenden Stadien:
- T0 – Anzeichen von Brustkrebs wurden nicht erkannt (nicht nachgewiesen).
- Die Bezeichnung Tis (Tumor in situ) bezieht sich auf Karzinome und wird wie folgt entschlüsselt: Es werden abnorme Zellen in situ gefunden (keine Invasion), die Lokalisation ist auf die Milchgänge (DCIS) oder Läppchen (LCIS) der Brustdrüse beschränkt. Es gibt auch Tis Paget, also die Paget-Krankheit, die das Gewebe der Brustwarze und des Warzenhofs befällt.
- T1 – der Tumordurchmesser an der breitesten Stelle beträgt 20 mm oder weniger:
- T1a – Tumordurchmesser > 1 mm, aber < 5 mm;
- T1b – Tumordurchmesser ist größer als 5 mm, aber kleiner als 10 mm;
- T1c – Tumordurchmesser >10 mm, aber ≤ 20 mm.
- T2 – Tumordurchmesser > 20 mm, aber < 50 mm.
- T3 – der Tumordurchmesser überschreitet 50 mm.
- T4 – der Tumor hat eine beliebige Größe und hat sich ausgebreitet: in die Brust (T4a), in die Haut (T4b), in Brust und Haut (T4c), entzündlicher Brustkrebs (T4d).

Lymphknotenindikatoren:
- NX – Lymphknoten können nicht beurteilt werden.
- N0 – In den Lymphknoten wurde kein Krebs gefunden.
- N0 (+) – In den Achsellymphknoten finden sich kleine Bereiche „isolierter“ Tumorzellen (weniger als 0,2 mm).
- N1mic – Bereiche von Tumorzellen in den Achsellymphknoten, die größer als 0,2 mm, aber kleiner als 2 mm sind (können nur unter dem Mikroskop sichtbar sein und werden oft als Mikrometastasen bezeichnet).
- N1 – Der Krebs hat sich auf 1-2-3 Achsellymphknoten (oder die gleiche Anzahl intrathorakaler Lymphknoten) ausgebreitet, maximale Größe 2 mm.
- N2 – der Krebs hat sich auf 4–9 Lymphknoten ausgebreitet: nur auf die Achsellymphknoten (N2a), nur auf die inneren Brustlymphknoten (N2b).
- N3 – der Krebs hat sich auf 10 oder mehr Lymphknoten ausgebreitet: auf die Lymphknoten unter dem Arm oder unter dem Schlüsselbein oder über dem Schlüsselbein (N3a); auf die inneren Brust- oder Achsellymphknoten (N3b); die supraklavikulären Lymphknoten sind betroffen (N3c).
Indikatoren für Fernmetastasen:
- M0 – keine Metastasen;
- M0 (+) – es gibt keine klinischen oder radiologischen Anzeichen von Fernmetastasen, aber Tumorzellen werden im Blut oder Knochenmark oder in anderen Lymphknoten nachgewiesen;
- M1 – Es werden Metastasen in anderen Organen festgestellt.
Histologische Klassifikation von Brustkrebs
Die aktuelle histopathologische Klassifizierung von Brustkrebs basiert auf den morphologischen Merkmalen von Neoplasien, die bei der histologischen Untersuchung von Tumorgewebeproben – Biopsien – untersucht werden.
In der aktuellen Version, die 2003 von der WHO genehmigt und weltweit akzeptiert wurde, umfasst diese Klassifikation etwa zwei Dutzend Haupttumortypen und fast ebenso viele weniger bedeutende (seltene) Subtypen.
Man unterscheidet folgende Haupthistotypen des Brustkrebses:
- nichtinvasiver (nicht infiltrierender) Krebs: intraduktales (duktales) Karzinom, lobuläres Karzinom (LCIS);
- invasiver (infiltrierender) Krebs: duktaler (intraduktaler) oder lobulärer Krebs.
Laut Statistiken der Europäischen Gesellschaft für Medizinische Onkologie (ESMO) machen diese Typen 80 % der klinischen Fälle von bösartigen Brusttumoren aus. In anderen Fällen werden weniger häufige Brustkrebsarten diagnostiziert, insbesondere: medullär (Weichteilkrebs); tubulärer (Krebszellen bilden röhrenförmige Strukturen); muzinös oder kolloidal (mit Schleim); metaplastisch (Plattenepithelkarzinom, glanduläres Plattenepithelkarzinom, adenoid-zystisch, mykoepidermoid); papillär, mikropapillär); Morbus Paget (Tumor der Brustwarze und des Warzenhofs) usw.
Anhand des standardmäßigen histologischen Untersuchungsprotokolls wird der Differenzierungsgrad (Unterscheidung) von Normal- und Tumorzellen bestimmt. Die histologische Klassifizierung von Brustkrebs ermöglicht somit die Bestimmung des Tumormalignitätsgrads (dies ist nicht dasselbe wie Krebsstadien). Dieser Parameter ist sehr wichtig, da der Grad der histopathologischen Differenzierung neoplastischen Gewebes Aufschluss über dessen invasives Wachstumspotenzial gibt.
Abhängig von der Anzahl der Abweichungen in der Zellstruktur werden Grade unterschieden (Grad):
- GX – Gewebeunterscheidungsgrad kann nicht beurteilt werden;
- G1 – der Tumor ist hochdifferenziert (niedriggradig), d. h. die Tumorzellen und die Organisation des Tumorgewebes sind nahezu normal;
- G2 – mäßig differenziert (Mittelstufe);
- G3 – gering differenziert (hochgradig);
- G4 – undifferenziert (hoher Grad).
Die Grade G3 und G4 weisen auf ein deutliches Überwiegen atypischer Zellen hin; solche Tumoren wachsen schnell und ihre Ausbreitungsrate ist höher als bei Tumoren mit Differenzierung auf G1- und G2-Niveau.
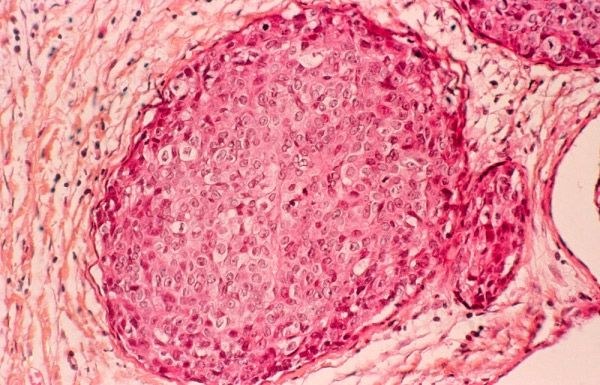
Die Hauptnachteile dieser Klassifikation liegen laut Experten in der eingeschränkten Fähigkeit, die Heterogenität von Brustkrebs genauer abzubilden, da eine Gruppe Tumoren mit völlig unterschiedlichen biologischen und klinischen Profilen umfasste. Daher hat die histologische Klassifikation von Brustkrebs nur einen minimalen prognostischen Wert.
Immunhistochemische Klassifikation von Brustkrebs
Dank der Verwendung neuer molekularer Tumormarker – der Expression von Tumorzellrezeptoren für Östrogen (ER) und Progesteron (PgR) sowie des Status von HER2 (transmembranöser Proteinrezeptor des epidermalen Wachstumsfaktors EGFR, der das Zellwachstum stimuliert) – ist eine neue internationale Klassifikation des Brustkrebses entstanden, die einen nachgewiesenen prognostischen Wert hat und eine genauere Bestimmung der Therapiemethoden ermöglicht.
Basierend auf dem Zustand der Östrogen- und Progesteronrezeptoren, deren Aktivierung zu Zellveränderungen und Tumorwachstum führt, unterscheidet die immunhistochemische Klassifizierung von Brustkrebs zwischen hormonpositiven (ER+, PgR+) und hormonnegativen (ER-, PgR-) Tumoren. Auch der Status der EGFR-Rezeptoren kann positiv (HER2+) oder negativ (HER2-) sein, was die Behandlungstaktik grundlegend beeinflusst.
Hormonpositiver Brustkrebs reagiert gut auf eine Hormontherapie mit Medikamenten, die den Östrogenspiegel senken oder dessen Rezeptoren blockieren. Diese Tumoren wachsen tendenziell langsamer als hormonnegative.
Mammologen weisen darauf hin, dass Patientinnen mit dieser Art von Neoplasie (die häufig nach der Menopause auftritt und das Gewebe entlang der Milchgänge befällt) kurzfristig eine bessere Prognose haben, Krebs mit ER+ und PgR+ jedoch manchmal nach vielen Jahren wiederkehren kann.
Hormonnegative Tumoren werden viel häufiger bei Frauen diagnostiziert, die die Wechseljahre noch nicht hinter sich haben. Diese Neoplasien werden nicht mit Hormonmedikamenten behandelt und wachsen schneller als hormonpositive Krebsarten.
Darüber hinaus unterscheidet die immunhistochemische Klassifizierung von Brustkrebs zwischen dreifach positivem Krebs (ER+, PgR+ und HER2+), der mit Hormonpräparaten und Medikamenten mit monoklonalen Antikörpern behandelt werden kann, die die Expression von HER2-Rezeptoren unterdrücken sollen (Herceptin oder Trastuzumab).
Der dreifach negative Krebs (ER-, PgR-, HER2-), der als molekularer basaler Subtyp klassifiziert wird, ist typisch für junge Frauen mit einem mutierten BRCA1-Gen; die wichtigste medikamentöse Behandlung besteht in der Zytostatika-Chemotherapie.
In der Onkologie ist es üblich, die Entscheidung über die Verschreibung einer Behandlung auf Grundlage aller möglichen Krankheitsmerkmale zu treffen, die jede Brustkrebsklassifizierung dem Arzt bietet.


 [
[