
Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Geschlossenes System zur Verabreichung von Medikamenten könnte die Verabreichung von Chemotherapie verbessern
Zuletzt überprüft: 02.07.2025
 ">
">Bei einer Chemotherapie wird die Dosis der meisten Medikamente anhand der Körperoberfläche des Patienten berechnet. Diese wird mithilfe einer Gleichung ermittelt, die Größe und Gewicht des Patienten berücksichtigt. Diese Gleichung wurde 1916 auf Grundlage der Daten von nur neun Patienten aufgestellt.
Dieser vereinfachte Dosierungsansatz berücksichtigt keine anderen Faktoren und kann dazu führen, dass ein Patient zu viel oder zu wenig von einem Medikament erhält. Infolgedessen kann es bei manchen Patienten zu unnötiger Toxizität oder unzureichender Wirksamkeit der Chemotherapie kommen.
Um die Dosierungsgenauigkeit von Chemotherapien zu verbessern, haben MIT-Ingenieure einen alternativen Ansatz entwickelt, der eine individuelle Dosierung für jeden Patienten ermöglicht. Ihr System misst die Medikamentenmenge im Körper des Patienten und leitet diese Daten an einen Controller weiter, der die Infusionsrate entsprechend anpassen kann.
Dieser Ansatz könne dazu beitragen, Unterschiede in der Pharmakokinetik von Medikamenten auszugleichen, die durch Körperzusammensetzung, genetische Veranlagung, durch Chemotherapie verursachte Organtoxizität, Wechselwirkungen mit anderen Medikamenten und Nahrungsmitteln sowie zirkadiane Schwankungen der Enzyme, die für den Abbau der Chemotherapeutika verantwortlich sind, verursacht würden, sagen die Forscher.
„Wir sind überzeugt, dass wir durch die Anerkennung der Fortschritte im Verständnis des Arzneimittelstoffwechsels und die Anwendung technischer Werkzeuge zur Vereinfachung der personalisierten Dosierung dazu beitragen können, die Sicherheit und Wirksamkeit vieler Medikamente zu verbessern“, sagte Giovanni Traverso, außerordentlicher Professor für Maschinenbau am MIT, Gastroenterologe am Brigham and Women’s Hospital und leitender Autor der Studie.
Louis DeRidder, ein Doktorand am MIT, ist der Hauptautor des im Fachjournal Med veröffentlichten Artikels.
Kontinuierliche Überwachung
In dieser Studie konzentrierten sich die Forscher auf das Medikament 5-Fluorouracil, das zur Behandlungvon Dickdarmkrebs und anderen Krebsarten eingesetzt wird. Das Medikament wird üblicherweise über einen Zeitraum von 46 Stunden verabreicht. Die Dosierung wird anhand einer Formel bestimmt, die auf Größe und Gewicht des Patienten basiert und so die Körperoberfläche des Patienten abschätzt.
Dieser Ansatz berücksichtigt jedoch keine Unterschiede in der Körperzusammensetzung, die die Verteilung des Medikaments im Körper beeinflussen können, oder genetische Variationen, die den Stoffwechsel beeinflussen. Diese Unterschiede können bei zu hoher Medikamentendosis zu schädlichen Nebenwirkungen führen. Wird zu wenig verabreicht, kann es sein, dass der Tumor nicht wie erwartet abgetötet wird.
„Menschen mit der gleichen Körperoberfläche können sehr unterschiedliche Größen und Gewichte, unterschiedliche Muskelmasse oder unterschiedliche genetische Anlagen haben, aber solange Größe und Gewicht in diese Gleichung eingesetzt werden und die gleiche Körperoberfläche ergeben, ist ihre Dosis identisch“, sagt DeRidder, ein Doktorand im Studiengang Medizintechnik und Medizinphysik am Harvard-MIT-Programm für Gesundheitswissenschaften und -technologie.
Ein weiterer Faktor, der die Medikamentenmenge im Blut zu einem bestimmten Zeitpunkt verändern kann, ist die zirkadiane Schwankung des Enzyms Dihydropyrimidin-Dehydrogenase (DPD), das 5-Fluorouracil abbaut. Die Expression von DPD wird, wie viele andere Enzyme im Körper, durch einen zirkadianen Rhythmus reguliert. Daher ist der Abbau von 5-FU durch DPD nicht konstant, sondern variiert mit der Tageszeit. Diese zirkadianen Rhythmen können während einer Infusion zu einer zehnfachen Schwankung der 5-FU-Menge im Blut eines Patienten führen.
„Da wir die Körperoberfläche zur Berechnung der Chemotherapiedosis heranziehen, wissen wir, dass 5-Fluorouracil bei zwei Personen sehr unterschiedlich toxisch wirken kann. Ein Patient kann Behandlungszyklen mit minimaler Toxizität durchlaufen, gefolgt von einem Zyklus mit extremer Toxizität. Von einem Zyklus zum nächsten hat sich die Art und Weise verändert, wie der Patient die Chemotherapie verstoffwechselt. Unsere veraltete Dosierungsmethode berücksichtigt diese Veränderungen nicht, und die Patienten leiden darunter“, sagt Douglas Rubinson, klinischer Onkologe am Dana-Farber Cancer Institute und Autor der Studie.
Eine Möglichkeit, die Variabilität der Pharmakokinetik der Chemotherapie auszugleichen, ist die sogenannte therapeutische Arzneimittelüberwachung. Dabei gibt der Patient am Ende eines Behandlungszyklus eine Blutprobe ab. Nach der Analyse der Arzneimittelkonzentrationen kann die Dosierung zu Beginn des nächsten Zyklus (bei 5-Fluorouracil in der Regel alle zwei Wochen) gegebenenfalls angepasst werden.
Dieser Ansatz hat sich als vorteilhaft für die Patienten erwiesen, wird jedoch bei Chemotherapien wie 5-Fluorouracil nicht häufig eingesetzt.
Die Forscher am MIT wollten eine ähnliche Art der Überwachung entwickeln, allerdings auf automatisierte Weise, die eine personalisierte Medikamentendosierung in Echtzeit ermöglichen würde, was zu besseren Ergebnissen für die Patienten führen könnte.
In ihrem geschlossenen Kreislaufsystem können die Arzneimittelkonzentrationen kontinuierlich überwacht werden und diese Informationen werden verwendet, um die Infusionsrate des Chemotherapeutikums automatisch anzupassen, um die Dosis im Zielbereich zu halten.
Dieses geschlossene System ermöglicht eine personalisierte Medikamentendosierung, bei der die zirkadianen Rhythmen der Arzneimittel-metabolisierenden Enzymwerte sowie alle Änderungen der Pharmakokinetik des Patienten seit der letzten Behandlung, wie beispielsweise eine durch die Chemotherapie verursachte Organtoxizität, berücksichtigt werden.
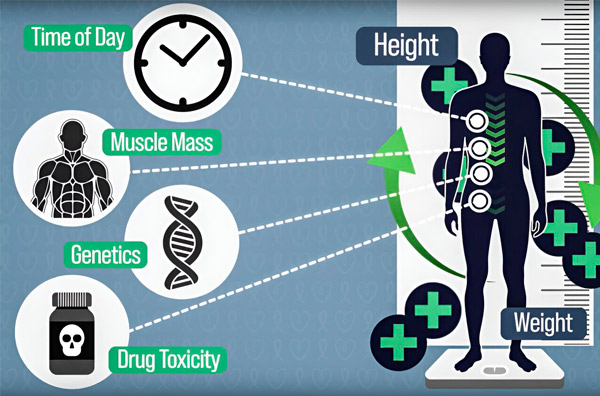
Um die Dosierung von Chemotherapien präziser zu gestalten, haben MIT-Ingenieure eine Methode entwickelt, die Medikamentenmenge im Körper eines Patienten während einer mehrstündigen Infusion kontinuierlich zu messen. Dies hilft, Unterschiede auszugleichen, die durch Körperzusammensetzung, Genetik, Medikamententoxizität und zirkadiane Schwankungen verursacht werden. Quelle: Mit freundlicher Genehmigung der Forscher.
Das neue System der Forscher, bekannt als CLAUDIA (Closed-Loop AUtomated Drug Infusion regulAtor), nutzt für jeden Schritt handelsübliche Geräte. Alle fünf Minuten werden Blutproben entnommen und schnell für die Analyse vorbereitet. Die Konzentration von 5-Fluorouracil im Blut wird gemessen und mit dem Zielbereich verglichen.
Die Differenz zwischen der Zielkonzentration und der gemessenen Konzentration wird in einen Steueralgorithmus eingegeben, der dann die Infusionsrate nach Bedarf anpasst, um die Dosis innerhalb des Konzentrationsbereichs zu halten, bei dem das Medikament wirksam und nicht toxisch ist.
„Wir haben ein System entwickelt, mit dem wir die Arzneimittelkonzentration kontinuierlich messen und die Infusionsrate entsprechend anpassen können, um die Arzneimittelkonzentration im therapeutischen Fenster zu halten“, sagt DeRidder.
Schnelle Anpassung
In Tierversuchen stellten die Forscher fest, dass sie mit CLAUDIA die im Körper zirkulierende Arzneimittelmenge in etwa 45 Prozent der Fälle im Zielbereich halten konnten.
Die Wirkstoffkonzentrationen von Tieren, die eine Chemotherapie ohne CLAUDIA erhielten, blieben durchschnittlich nur in 13 Prozent der Fälle im Zielbereich. Die Forscher prüften die Wirksamkeit der Wirkstoffkonzentrationen in dieser Studie nicht, aber es wird angenommen, dass die Aufrechterhaltung der Konzentrationen im Zielbereich zu besseren Ergebnissen und geringerer Toxizität führt.
CLAUDIA konnte die 5-Fluorouracil-Dosis auch dann im Zielbereich halten, wenn ein Medikament verabreicht wurde, das das DPD-Enzym hemmt. Bei Tieren, die diesen Hemmer ohne kontinuierliche Überwachung und Anpassung erhielten, stiegen die 5-Fluorouracil-Spiegel um das bis zu Achtfache.
Für diese Demonstration führten die Forscher jeden Schritt des Prozesses manuell mit handelsüblicher Ausrüstung durch. Nun planen sie jedoch, jeden Schritt zu automatisieren, sodass die Überwachung und Dosisanpassung ohne menschliches Eingreifen erfolgen kann.
Zur Messung der Arzneimittelkonzentrationen verwendeten die Forscher die Hochleistungsflüssigkeitschromatographie-Massenspektrometrie (HPLC-MS), eine Technik, die zur Erkennung nahezu aller Arzneimitteltypen angepasst werden kann.
„Wir sehen eine Zukunft, in der wir CLAUDIA für jedes Medikament verwenden können, das die entsprechenden pharmakokinetischen Eigenschaften aufweist und durch HPLC-MS nachweisbar ist, was eine personalisierte Dosierung für viele verschiedene Medikamente ermöglicht“, sagt DeRidder.
