
Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Krebszellen aktivieren sofort die Energieproduktion, wenn die DNA komprimiert und beschädigt wird
Zuletzt überprüft: 03.08.2025
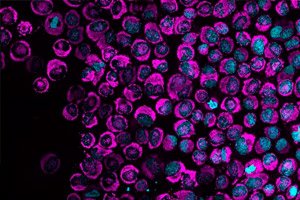
Krebszellen aktivieren laut einer im Fachmagazin Nature Communications veröffentlichten Studie sofort eine energiereiche Reaktion auf physischen Druck. Dieser Energieschub ist die erste dokumentierte Manifestation eines Schutzmechanismus, der Zellen hilft, beschädigte DNA zu reparieren und die beengten Verhältnisse im menschlichen Körper zu überleben.
Diese Erkenntnisse helfen zu erklären, wie Krebszellen in komplexen mechanischen Umgebungen überleben, beispielsweise indem sie durch Tumormikroumgebungen kriechen, poröse Blutgefäße durchdringen oder Schocks im Blutkreislauf überwinden. Die Entdeckung des Mechanismus könnte zu neuen Strategien führen, um Krebszellen zu „verankern“, bevor sie sich ausbreiten.
Forscher am Centre for Genomic Regulation (CRG) in Barcelona machten die Entdeckung mithilfe eines Spezialmikroskops, mit dem sich lebende Zellen auf eine Breite von nur drei Mikrometern zusammendrücken lassen – etwa dreißigmal kleiner als der Durchmesser eines menschlichen Haares. Sie beobachteten, dass die Mitochondrien in HeLa-Zellen innerhalb weniger Sekunden nach der Komprimierung an die Oberfläche des Zellkerns strömten und begannen, zusätzliches ATP, die molekulare Energiequelle der Zellen, in den Zellkern zu pumpen.
„Das zwingt uns, die Rolle der Mitochondrien im menschlichen Körper zu überdenken. Sie sind nicht nur statische Batterien, die Zellen mit Energie versorgen, sondern vielmehr clevere ‚Retter‘, die im Notfall gerufen werden können, wenn eine Zelle buchstäblich an ihre Grenzen stößt“, sagt Dr. Sarah Sdelchy, eine Co-Autorin der Studie.
Die Mitochondrien bildeten ein so dichtes „Leuchten“ um den Zellkern, dass dieser nach innen gedrückt wurde. Dieses Phänomen wurde bei 84 Prozent der komprimierten HeLa-Krebszellen beobachtet, während es bei den schwimmenden, unkomprimierten Zellen fast null war. Die Forscher nannten diese Strukturen NAM (Nucleus-associated mitochondria).
Um herauszufinden, was die NAMs tun, verwendeten die Forscher einen Fluoreszenzsensor, der aufleuchtet, wenn ATP in den Zellkern gelangt. Bereits drei Sekunden nach dem Zusammendrücken der Zellen verstärkte sich das Signal um etwa 60 Prozent.
„Dies ist ein klares Zeichen dafür, dass sich die Zellen an den Stress anpassen und ihren Stoffwechsel umstellen“, erklärt Dr. Fabio Pezzano, erster Co-Autor der Studie.
Weitere Experimente zeigten, warum dieser Energieschub wichtig ist. Mechanische Kompression belastet die DNA, bricht Stränge und verwickelt das Genom. Zellen benötigen ATP-abhängige Reparaturkomplexe, um die DNA-Struktur zu schwächen und den Schaden zu beseitigen. Komprimierte Zellen, die zusätzliches ATP erhielten, reparierten ihre DNA innerhalb weniger Stunden, während Zellen ohne zusätzliches ATP ihre normale Teilung einstellten.
Um die Bedeutung dieses Mechanismus für die Erkrankung zu bestätigen, untersuchten die Forscher auch Brusttumorbiopsien von 17 Patientinnen. NAM-Halos wurden in 5,4 % der Kerne am invasiven Rand des Tumors beobachtet, verglichen mit 1,8 % im dichten Kern – ein dreifacher Unterschied.
„Die Tatsache, dass wir diese Signatur im Patientengewebe gefunden haben, bestätigte ihre Bedeutung außerhalb des Labors“, erklärt Dr. Ritobrata (Rito) Ghose, der erste Co-Autor der Studie.
Die Forscher untersuchten auch die zellulären Mechanismen, die die mitochondriale „Flut“ ermöglichen. Aktinfilamente – dieselben Proteinfäden, die Muskelkontraktionen ermöglichen – bilden einen Ring um den Zellkern, und das endoplasmatische Retikulum zieht die netzartige „Falle“ zusammen. Diese kombinierte Anordnung, so zeigte die Studie, hält NAM physisch an Ort und Stelle und bildet einen „Heiligenschein“. Als die Forscher die Zellen mit Latrunculin A behandelten, einem Medikament, das Aktin hemmt, verschwand die NAM-Bildung und der ATP-Spiegel sank drastisch.
Wenn metastatische Zellen auf NAM-assoziierte ATP-Ausbrüche angewiesen sind, könnten Medikamente, die das Gerüst zerstören, Tumore weniger invasiv machen, ohne die Mitochondrien selbst zu vergiften oder gesundes Gewebe zu beeinträchtigen.
„Mechanische Stressreaktionen sind eine noch wenig erforschte Schwachstelle von Krebszellen, die neue Therapieansätze eröffnen könnte“, sagt Dr. Verena Ruprecht, Co-Autorin der Studie.
Obwohl sich die Studie auf Krebszellen konzentrierte, weisen die Autoren darauf hin, dass es sich dabei wahrscheinlich um ein universelles Phänomen in der Biologie handelt. Immunzellen, die durch Lymphknoten wandern, Neuronen im Wachstumsprozess und embryonale Zellen während der Morphogenese erfahren alle ähnliche physische Belastungen.
„Wenn Zellen unter Druck stehen, schützt der Energieschub zum Zellkern wahrscheinlich die Integrität des Genoms“, schlussfolgert Dr. Sdelchi. „Dies ist eine völlig neue Ebene der Regulierung in der Zellbiologie und stellt einen grundlegenden Wandel in unserem Verständnis dar, wie Zellen physischen Stress überleben.“
