
Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Fusobakterien: Freund oder Feind?
Facharzt des Artikels
Zuletzt überprüft: 06.07.2025
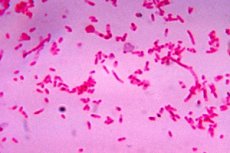
Nach der in der Mikrobiologie anerkannten Klassifikation sind Fusobakterien Prokaryoten und gramnegative anaerobe Bakterien, die im Körper von Menschen und anderen Säugetieren leben und Teil der konstanten normalen Mikrobiozönose oder Mikroflora sind. Ihre Familie - Fusobacteriaceae - umfasst mehr als anderthalb Dutzend Arten.
Morphologie von Fusobakterien und Merkmale ihres Stoffwechsels
Fusobakterien haben aufgrund ihrer beidseitig spitzen Enden eine einzellige, spindelförmige Struktur (lateinisch „fusus“). Die Stäbchen können dick und dünn, gerade und gebogen sowie fadenförmig sein. Die Länge dieser Bakterien liegt zwischen 0,0005 und 0,008 mm. Sie besitzen keine Bewegungsorgane, obwohl einige Quellen behaupten, sie hätten peritriche (über die gesamte Oberfläche verteilte) Geißeln.
Bakteriologen stellen fest, dass diese Mikroorganismen keine Sporen bilden, das heißt, bei einer Verschlechterung der Lebensbedingungen können sie sich nicht in Zellen mit einer dichten Membran verwandeln. Fusobakterien vermehren sich durch mitotische Spaltung einer Zelle in zwei mit horizontalem Transfer von im Nukleoid konzentrierten Genen.
Die Morphologie der Fusobakterien bestimmt teilweise den Lebensraum ihrer Kolonien: die Schleimhäute der Mundhöhle, der Atemwege, des Urogenitalbereichs und des unteren Teils des Verdauungstrakts – des Dickdarms. Ihr Vorkommen im Blut ist nicht nachgewiesen, Fusobakterien benötigen dies jedoch nicht, da sie ihre Nährstoffe durch die Ölfermentation von Glucose, Saccharose, Maltose und einigen Aminosäuren erhalten.
Der Stoffwechsel dieser Mikroorganismen basiert auf dem biochemischen Prozess der anaeroben (sauerstofffreien) Zersetzung von Kohlenhydraten unter dem Einfluss von Enzymen. Die Metabolite sind niedermolekulare Buttersäure, Kohlendioxid und Wasserstoff. Zur Energiegewinnung benötigen Bakterien Wasserstoff. Dessen Ionen werden vom Oberflächenprotein des Fusobakterien-Adhäsins A (FadA) aufgenommen und in die Zelle transportiert.
Buttersäure ist übrigens sehr wichtig für die Aufrechterhaltung der Darmhomöostase (Aufnahme von Wasser und Elektrolyten) und für die Regeneration von Schleimhautepithelzellen. Ärzte haben einen Zusammenhang zwischen dem Mangel dieser Säure im Darm und der Entwicklung lokaler entzündlicher Erkrankungen (z. B. Colitis ulcerosa) festgestellt. Neben Fusobakterien wird Buttersäure von Bakterien der Gattung Clostridium produziert.
Zur bedingten Pathogenität von Fusobakterien
Fusobakterien gelten wie die meisten gramnegativen Anaerobier unter Bakteriologen als opportunistische Krankheitserreger. Es gibt jedoch Stämme, an deren erhöhter Pathogenität Wissenschaftler nicht mehr zweifeln. Dazu gehören insbesondere Fusobacterium necrophorum, das in der Mundhöhle und im Darm lebt, und Fusobacterium nucleatum, das Zahnbelag als Lebensraum gewählt hat.
Wie funktioniert ihr pathogener Mechanismus? Die äußere Oberfläche der zytoplasmatischen Membran von Fusobakterien besteht aus polymerisierten Fetten, Proteinen und Kohlenhydraten in Form von Lipopolysacchariden, die bakterielle Giftstoffe (Endotoxine) und gleichzeitig Antigene sind. Das heißt, diese Verbindungen lösen eine Immunantwort des Körpers und eine Entzündungsreaktion aus, ohne dass eine offensichtliche exogene (äußere) Einwirkung auf einzelne Systeme und Organe vorliegt.
Es besteht die Meinung, dass sich die Pathogenität einiger Bakterien der Familie Fusobacteriaceae nur bei geschwächter Immunität manifestiert. Es sollte jedoch berücksichtigt werden, dass sie nachweislich sehr aggressiv sein können, da Fusobakterien Phospholipase A produzieren - ein Enzym, das Lipide von Zellmembranen abbaut und Bakterien den Zugang zu Zellen aller Gewebe öffnet. Mikroorganismen verwenden dieses Enzym jedoch in der Regel nicht "allein", sondern in Gegenwart pathogener Mikroorganismen nimmt die Aktivität signifikant zu. Wenn die Schleimhaut durch Streptokokken oder Staphylokokken geschädigt wird, nutzen Fusobakterien die Gelegenheit, dringen tiefer ein und verursachen eine nekrotische Entzündung des Gewebes. Das anschaulichste Beispiel für einen solchen synergistischen Effekt ist die gangränöse Pharyngitis (oder Simanovsky-Plaut-Vincent-Angina), die aufgrund einer Infektion der Schleimhaut durch die gramnegativen Spirochaetales-Bakterien Borrelia vincentii, Prevotella intermedia und Fusobacterium nucleatum auftritt.
Welche Krankheiten werden durch Fusobakterien verursacht?
Lassen Sie uns nun einige Krankheiten auflisten, die durch Fusobakterien verursacht werden, oder genauer gesagt Pathologien, die sich unter ihrer mehr als aktiven Beteiligung entwickeln. Ärzte zählen dazu Folgendes:
- Pulpitis kariöser Zähne;
- Zahnfleischentzündung;
- Parodontitis (Parodontitis);
- Osteomyelitis des Kiefers;
- Phlegmonen verschiedener Lokalisationen;
- Mandelentzündung und Paratonsillitis (phlegmonöse Mandelentzündung);
- chronische Sinusitis;
- Retropharyngealabszess nach Streptokokken-Tonsillitis mit Nekrose und Sepsis (Lemierre-Syndrom);
- Bronchiektasie;
- eitrige Lungenentzündung;
- Lungenabszess;
- Empyem der Pleura;
- Hirnabszesse;
- eitrige Entzündung der Bauchorgane;
- erosive Balanitis und Balanoposthitis;
- akute Kolpitis (Vaginitis) und Vulvitis;
- eitrig-septische Komplikationen bei medizinischen Abtreibungen;
- Colitis ulcerosa;
- Morbus Crohn;
- Septikämie.
Forscher der Harvard Medical School und des Dana-Faber Cancer Institute führten eine Genomanalyse von Darmkrebstumoren durch und fanden darin eine ungewöhnlich hohe Anzahl von Fusobakterien F. nucleatum. Derzeit laufen Studien, um die Hypothese zu bestätigen (oder zu widerlegen), dass Fusobakterien an der Entstehung von Dickdarm- und Mastdarmkrebs beteiligt sind. Tatsache ist, dass das oben erwähnte bakterielle Oberflächenprotein Adhäsin A an das Transmembranglykoprotein menschlicher Epithelzellen, E-Cadherin, bindet. Dieses Protein sorgt für die interzelluläre Adhäsion in unserem Gewebe und kann Krebszellen zusammenkleben, wodurch deren Invasion verhindert wird. Fusobakterien neutralisieren es jedoch, wodurch die ungehinderte Vermehrung von Krebszellen beginnt. [ 4 ], [ 5 ]
Behandlung von Fusobakterien
Die Behandlung von Fusobakterien bzw. die medikamentöse Therapie von Fusobakterienerkrankungen erfolgt mit Antibiotika.
Unter den antibakteriellen Medikamenten bevorzugen Ärzte diejenigen, die am wirksamsten gegen F. nucleatum und F. necrophorum sind: Clindamycin, Carbenicillin, Cefoxitin, Cefoperazon, Cefamandol, Fosfimycin, Ornidazol. Die Verschreibung eines bestimmten Medikaments hängt natürlich von der Diagnose und dem klinischen Bild der Erkrankung ab.
Carbenicillin (Handelsnamen: Carbecin, Fugacillin, Microcillin, Pyocyanil usw.) wirkt nur auf gramnegative Bakterien und wird im Rahmen einer komplexen Therapie bei Peritonitis, Septikämie, Meningitis und Osteomyelitis eingesetzt.
Das Cephalosporin-Antibiotikum Cefoxitin (Mefoxin, Atralxitin, Boncefin) der zweiten Generation wird für eine breite Palette von Erkrankungen bakterieller Ätiologie empfohlen, darunter Mandelentzündung, Lungenentzündung, Harnwegsinfektionen, Knochen-, Gelenk-, Haut- und Weichteilinfektionen; es wird verschrieben, um infektiösen Komplikationen nach Operationen vorzubeugen.
Und das Medikament Fosfomycin (Fosfomycin-Trometamol, Monural, Urofosfabol) wird bei urologischen Bakteriosen eingesetzt – rezidivierende Blasenentzündungen oder unspezifische Urethritis (Einzeldosis 3 g).
Zu Beginn des Artikels haben wir versprochen, den Grad der Gefährlichkeit des winzigen einzelligen Fusobakteriums für den Menschen herauszufinden. Ja, es kann pathogen sein, aber andererseits kann der Mensch seine Anwesenheit in der Mikroflora nicht loswerden.


 [
[