
Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
„Intelligentes“ Hydrogel für diabetische Wunden: antiseptisch, entzündungshemmend und Hilfe bei Zucker
Zuletzt überprüft: 09.08.2025
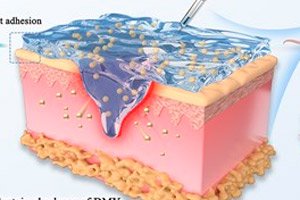 ">
">Diabetische Wunden, insbesondere Fußgeschwüre, heilen langsam: Infektionen (MRSA und andere), ein Überschuss an reaktiven Sauerstoffspezies (ROS), anhaltende Entzündungen, schlechtes Gefäßwachstum und chronisch erhöhte Blutzuckerwerte verhindern die Regeneration der Haut. Es gibt keine einfache Lösung – es bedarf eines Systems, das mehrere Probleme gleichzeitig löst. Die Studie wurde in der Fachzeitschrift Burns and Trauma veröffentlicht.
Was ist Ihnen eingefallen?
Die Forscher entwickelten ein DPFI-Hydrogel, im Wesentlichen ein „intelligentes Pflaster“, das mit einer Spritze injiziert werden kann. Es enthält das natürliche Flavonoid Dihydromyricetin (DMY), verpackt in PF127-CHO-Polymermizellen, und das Gel selbst ist mit PEI-Polymer vernetzt. Diese Zusammensetzung bietet drei wichtige Eigenschaften:
- Antibakterielle Wirkung ab den ersten Minuten (durch PEI).
- Langfristige Gewebe-„Fütterung“ von DMY: Es neutralisiert ROS, verschiebt Makrophagen vom Entzündungsprofil M1 zum „Reparaturprofil“ M2, reduziert die Konzentration entzündungsfördernder Zytokine und unterstützt das Gefäßwachstum und die Epithelisierung.
- Bonus für den Glukosestoffwechsel: DMY ist als Verbindung bekannt, die bei der Kontrolle von Hyperglykämie hilft – im Modell verbesserte es den „Zuckerhintergrund“ der Heilung.
Wie funktioniert das in der Praxis?
Gel:
- Haftet an feuchtem Stoff, heilt nach Verformung von selbst, geht durch eine Nadel (Scherverflüssigung) und gibt langsam DMY frei.
- In Zelltests unterdrückte es das Wachstum von MRSA und E. coli, reduzierte ROS stark, „löschte“ Entzündungen (senkte IL-6/IL-1β/TNF-α, erhöhte IL-10/IL-4), beschleunigte die Migration von Fibroblasten und die Bildung von „Röhren“ durch das Endothel (Gefäßrudimente).
- In Experimenten an diabetischen Mäusen mit MRSA-infizierten Wunden beschleunigte es den Heilungsprozess: Am 15. Tag führte eine der Formeln zu einer Heilung von etwa 97 % (gegenüber etwa 65 % ohne Behandlung), einer verbesserten Kollagenbildung und einem mikrovaskulären Wachstum und einer Senkung des Blutzuckerspiegels während der Heilung.
Wie unterscheidet sich dieser Verband vom üblichen?
Herkömmliche Hydrogele bilden im Grunde eine feuchte Umgebung und eine Barriere. Hier gibt es eine programmierbare Plattform: zunächst ein Angriff auf Mikroben, dann eine antioxidative und entzündungshemmende Blockade und schließlich die Unterstützung des Wachstums von Blutgefäßen und Epithel. Hinzu kommt eine Wirkung auf den Blutzucker, die insbesondere bei diabetischen Wunden wichtig ist.
Wo liegen die Fallstricke?
Alles wird in vitro und an Mäusen gezeigt. Vor der Klinik müssen Sie:
- die Sicherheit bestätigen (PEI unterliegt Toxizitätsbeschränkungen – Dosierung und Form sind wichtig),
- die Bioverfügbarkeit und Stabilität von DMY in realen Verbänden zu testen,
- Führen Sie große Tierversuche und anschließend klinische Studien zu Fußgeschwüren durch.
Kommentare der Autoren
Zur Neuheit der Plattform:
„Unseres Wissens ist DPFI das erste Hydrogel, das DMY + PEI + PF127-CHO gezielt zu einem multifunktionalen Rahmen mit programmierbarer Wirkung kombiniert.“Warum „Programmierbarkeit“?
Die Autoren betonen die Wirkungsabfolge: schnelle bakterielle Unterdrückung (PEI) → ROS-Clearance und Entzündungshemmung (DMY, M1→M2-Umschaltung) → Stimulation der Angiogenese/Epithelisierung bei gleichzeitiger Modulation der Glykämie.
„DPFI bietet eine sequenzielle Therapie, die auf Schlüsselknoten der diabetischen Wundheilung abzielt.“Multi-Target-Wirkung bestätigt.
„Umfassende In-vitro- und In-vivo-Tests zeigten die antibakteriellen, antioxidativen und entzündungshemmenden Eigenschaften von DPFI sowie die Unterstützung der Zellproliferation, Vaskularisierung und Glukoseregulation.“Zum klinischen Potenzial:
„DPFI ist eine vielversprechende integrative Strategie zur verbesserten Behandlung chronischer diabetischer Wunden und verdient eine weitere Erforschung für die klinische Anwendung.“Über die „Dosis als Werkzeug“.
Laut den Autoren unterdrückt ein höherer DMY-Gehalt Entzündungen und Bakterienlast stärker, während ein niedrigerer die Angiogenese besser unterstützt. Eine Lastoptimierung für die Heilungsphase ist erforderlich.Zur Sicherheit:
Die Autoren weisen auf eine gute Biokompatibilität (Hämolyse < 5 % nach ISO), keine erkennbare Toxizität in tierischen Organen und die haftenden und selbstheilenden Eigenschaften des Gels hin, die für Verbände geeignet sind.Einschränkungen und nächster Schritt:
„Die Ergebnisse liegen in Zellen und Mäusen vor; es sind Studien an großen Tieren, pharmakokinetische/Stabilitätsstudien, eine Feinabstimmung der Formulierung (einschließlich der potenziellen Toxizität von PEI) und dann frühe klinische Studien (z. B. bei Fußgeschwüren) erforderlich.“
Zusammenfassung
DPFI ist ein vielversprechender „Multitool“-Verband für komplexe diabetische Wunden: Er bekämpft gleichzeitig Bakterien, lindert oxidativen und entzündlichen Stress, unterstützt das Gefäßwachstum und hilft, den Blutzuckerspiegel unter Kontrolle zu halten. Von einem Erste-Hilfe-Kasten ist es zwar noch weit entfernt, aber das Konzept erscheint logisch für ein Problem, bei dem eine Maßnahme fast nie ausreicht.
