
Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Myokardiale Akinese
Facharzt des Artikels
Zuletzt überprüft: 12.07.2025
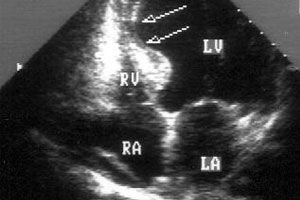
Bei der Diagnose von Herzerkrankungen kann eine Myokardakinese festgestellt werden, also die Unbeweglichkeit oder Unfähigkeit bestimmter Bereiche des Herzmuskelgewebes, sich zusammenzuziehen.
Somit ist die Myokardakinese keine Krankheit, sondern ein pathologischer Zustand, eine Störung der normalen motorischen Funktion des Herzmuskels, die durch Ultraschalldiagnostik des Herzens festgestellt wird und eines der strukturellen und funktionellen Anzeichen einer Reihe von Erkrankungen des Herz-Kreislauf-Systems ist.
Ursachen myokardiale Akinesie
Warum hört der Herzmuskel auf, sich zusammenzuziehen, d. h. was sind die Ursachen einer Myokardakinese?
In der kardiologischen Praxis wird die Pathogenese des Verlusts der normalen kontraktilen Funktion des Myokards (die bekanntlich von einem gesunden Herzen automatisch ausgeführt wird) am häufigsten mit einem Myokardinfarkt und der daraus resultierenden Nekrose eines Teils der arbeitenden Kardiomyozyten in Verbindung gebracht. Reparative Veränderungen (Remodellierung) des Myokards nach einem Infarkt führen zunächst zu einer Vergrößerung der Infarktzone, dann zu einer Verformung und Ausdehnung der Ventrikel, wobei sich die kardiomyozytäre Nekrosezone in eine Narbe verwandelt und einen Bereich myokardialer Akinese bildet. Fibröse Veränderungen können auch das die Ventrikel trennende Septum betreffen, und dann zeigt die Ultraschalluntersuchung eine Akinese im Bereich des interventrikulären Septums.
Ein Myokardinfarkt ist ein akuter Zustand einer Herzischämie oder ischämischen Herzkrankheit (IHK), der entsteht, wenn die Blutzirkulation im Koronararteriensystem gestört ist, was zu einer Myokardhypoxie und dem Absterben seiner Zellen führt.
Bei einer postinfarktbedingten Ausdünnung der Herzmuskelmembran und ihrer Ausstülpung – einem Aneurysma – zeigt die Ultraschallkardiographie eine Akinese der linken Herzkammer. Bei fast zwei Dritteln der Patienten kommt es zur Bildung eines Aneurysmas in der linken Herzkammer – an der Vorderwand oder an der Herzspitze, wobei auch hier eine Akinese der Herzspitze festgestellt wird.
Darüber hinaus besteht eine Korrelation zwischen den Ergebnissen der Echokardiographie, die eine Myokardakinesie sichtbar machen, und dem Postinfarkt-Myokardsyndrom – einer fokalen oder diffusen Postinfarkt-Kardiosklerose mit charakteristischem Ersatz geschädigter Kardiomyozyten durch Bindegewebe sowie mit einer Schädigung des Reizleitungssystems des Herzens (beeinträchtigte Weiterleitung bioelektrischer Impulse durch Zellen des Sinus- oder Atrioventrikularknotens).
Bei einer Myokarddegeneration bzw. -dystrophie, die ein der Kardiosklerose ähnliches histomorphologisches Bild aufweist, zeigen sich ebenfalls Veränderungen in der Struktur des Herzmuskelgewebes, die eine fokale Myokardakinesie nachweisen.
Häufig kommt es zu Schäden an den Zellen des Sinusknotens mit einer Abnahme der Bewegungsamplitude der Muskelwand und dem Fehlen ihrer Kontraktion, also einer Kombination aus Hypokinese und Akinese bei Patienten mit infektiöser Myokarditis. Diese Erkrankung kann mit der Bildung von entzündlichen Infiltraten im Interstitium und einer lokalisierten Myozytolyse aufgrund einer Entzündung durch Viren (Adeno- und Enterovirus, Picornaviridae, Coxsackie-Virus, Parvovirus B, Rötelnvirus, HSV-6), Bakterien (Corynebacterium diphtheriae, Haemophilus influenzae, Borrelia burgdorferi, Mycoplasma pneumoniae) sowie Protozoen (Trypanosoma cruzi, Toxoplasma gondii), Pilzen (Aspergillus) oder Parasiten (Ascaris, Echinococcus granulosus, Paragonimus westermani usw.) einhergehen. Wie klinische Statistiken zeigen, werden die meisten Fälle einer infektiösen Myokarditis durch Diphtherie, Grippe, Enteroviren und Toxoplasmose verursacht.
Und bei einer Myokarditis mit Autoimmunätiologie (assoziiert mit systemischem Lupus erythematodes, Sklerodermie, rheumatoider Arthritis, Morbus Whipple usw.) kann es zu einer Akinese des linken Ventrikels und seiner Funktionsstörung kommen, die mit lebensbedrohlichen Arrhythmien verbunden ist.
Unabhängig davon unterscheiden Kardiologen die Stresskardiomyopathie (Takotsubo-Kardiomyopathie), die von einheimischen Spezialisten als Broken-Heart-Syndrom bezeichnet wird. Diese plötzliche vorübergehende systolische Dysfunktion der mittleren apikalen Segmente des linken Ventrikels tritt häufig in Stresssituationen bei älteren Frauen auf, bei denen in der Vergangenheit keine koronare Herzkrankheit aufgetreten ist. Insbesondere wird an der Basis des linken Ventrikels eine Hyperkinesezone und darüber eine Akinese der Herzspitze festgestellt. Außerdem können Diagnostiker im Ultraschall des Herzens einen Bewegungsmangel im Bereich des interventrikulären Septums feststellen.
Risikofaktoren
Die Hauptrisikofaktoren für Störungen der normalen motorischen Funktion von Herzmuskelbereichen in Form einer Myokardakinesie sind die Entwicklung einer ischämischen Herzkrankheit. Als Risikofaktoren für seine Entwicklung gelten wiederum:
- Alter über 45 Jahre für Männer und über 55 Jahre für Frauen;
- frühe Herzerkrankungen in der Familienanamnese;
- verringerte Konzentrationen des Cholesterin transportierenden HDL-Proteins (High-Density-Lipoproteine) im Blut und erhöhte Konzentrationen des Low-Density-Lipoproteins (LDL), das zur Ablagerung von Cholesterin an den Wänden der Blutgefäße beiträgt – Arteriosklerose;
- hohe Triglyceridwerte im Blut (ernährungsbedingt);
- Bluthochdruck;
- Stoffwechselstörung (metabolisches Syndrom), die zu erhöhtem Blutdruck und Cholesterinablagerungen in den Herzkranzgefäßen beiträgt;
- Rauchen (einschließlich Passivrauchen), Fettleibigkeit, Bewegungsmangel, psychischer Stress und Depressionen.
Virale und bakterielle Infektionen des Myokards sowie Autoimmunerkrankungen lösen einen Risikofaktor für Myokardischämie aus, beispielsweise einen Anstieg des C-reaktiven Proteins (CRP) im Blut. Und der normale Zustand der Herzgefäße wird durch ein Ungleichgewicht der Gewebeplasminogenaktivatoren (tPA) und ihrer Inhibitoren (PAI) gestört, wodurch die Gefahr einer Thrombose der Koronarvenen mit deren vollständigem Verschluss besteht.
Pathogenese
Es wird vermutet, dass die Pathogenese dieser Kardiomyopathie in der unzureichenden Reaktion der Herzgefäße (Koronararterien und/oder Arteriolen und Kapillaren) auf die Freisetzung von Katecholamin-Neurotransmittern ins Blut liegt und dass es aufgrund der dadurch verursachten Vasospasmen zu kurzfristigen Anomalien der Myokardkontraktion kommt.
Symptome myokardiale Akinesie
Bei einer Myokardakinese – einem echokardiographischen Zeichen für Herz-Kreislauf-Erkrankungen – wird das klinische Bild durch die Symptome dieser Erkrankungen bestimmt. Dazu gehören: Kurzatmigkeit, Schmerzen unterschiedlicher Intensität im Herzbereich, Arrhythmie (Vorhof- oder Kammerrhythmusstörungen), Kammerflattern und Ohnmacht.
So klagen Patienten bei der Takotsubo-Kardiomyopathie am häufigsten über Schmerzen hinter dem Brustbein (mit drückender Natur), die in das linke Schulterblatt ausstrahlen, und über ein Gefühl von Luftmangel beim Einatmen.
Und Schmerzen bei Myokarditis können sowohl akut als auch anhaltend (ohne Wirkung bei Verwendung von Nitroglycerin) und gedämpft (Quetschen) sein. Darüber hinaus umfassen Herzsymptome bei dieser Krankheit infektiösen Ursprungs Kurzatmigkeit, Fieber, erhöhte Herzfrequenz und Herzflattern; blitzschnelle hämodynamische Störungen (ein Abfall der Blutflussvolumengeschwindigkeit), Bewusstlosigkeit und plötzlicher Herztod sind möglich.
Komplikationen und Konsequenzen
Sicherlich stellt die Myokardakinese im Vergleich zur Dyskinesie des postinfarktbedingten Narbenbereichs eine größere Gefahr für das Leben von Patienten mit Myokardinfarkt dar. Studien haben gezeigt, dass in etwa 40 % der Infarktfälle mit Koronargefäßverschluss die Myokardkontraktilität bei rechtzeitiger Wiederherstellung des Blutflusses im ischämischen Segment (Reperfusion) innerhalb von zwei bis sechs Wochen nach dem Infarkt wiederhergestellt wird. Zu den Folgen und Komplikationen zählen jedoch eine plötzliche Herzbeuteltamponade, elektromechanische Dissoziation und Tod.
Die Folgen und Komplikationen dystrophischer Veränderungen des Myokards mit seiner partiellen Akinese führen zu einer fast unvermeidlichen Atrophie der Muskelfasern, die sich nicht nur in Arrhythmien und einer Abnahme des systolischen Auswurfs, sondern auch in einer Erweiterung der Herzkammern mit chronischem Kreislaufversagen äußern kann.
Eine linksventrikuläre Akinese mit ihrer systolischen Dysfunktion und Herzinsuffizienz gehören zu den stärksten Prädiktoren für das Risiko eines plötzlichen Herztodes.
 [ 23 ]
[ 23 ]
Diagnose myokardiale Akinesie
Nur die instrumentelle Diagnostik des Myokards mittels Ultraschalluntersuchung des Herzens – Echokardiographie – ermöglicht es, Bereiche seiner Akinese zu identifizieren.
Eine spezielle Methode zur automatischen segmentalen Analyse der Herzkontraktionen ermöglicht die Verfolgung und Aufzeichnung aller Bewegungen der Herzwand.
Was muss untersucht werden?
Differenzialdiagnose
Zur Differentialdiagnose von Brustschmerzen – bei Patienten mit atypischem Krankheitsbild oder diagnostisch unklarem EKG-Befund – kommt auch die Echokardiographie zum Einsatz.
Bei Patienten ohne Myokardbewegungsstörung können mithilfe der Echokardiographie andere lebensbedrohliche Erkrankungen mit ähnlichem Krankheitsbild erkannt werden: eine massive Lungenembolie oder eine Aortendissektion.
Darüber hinaus umfasst die Diagnostik des Myokards, auch bei Störungen seiner kontraktilen Funktion, Blutuntersuchungen auf BSG, C-reaktives Protein, Antikörper (serologische Serumanalyse auf IgM-Spiegel), Elektrolytwerte und die Bestimmung von Markern für Myokardschäden (Troponin I- und T-Isoenzyme, Kreatinkinase).
Die Patienten werden einem Elektrokardiogramm (EKG), einer Röntgenkontrast-Koronarangiographie, einer tomographischen Szintigraphie (mit Radioisotopen), einer Farbdopplersonographie und einer Magnetresonanztomographie (MRT) unterzogen. Die Diagnose von Herzaneurysmen erfordert den Einsatz einer Röntgenkontrast-Ventrikulographie.
In manchen Fällen ist eine Differentialdiagnose des Myokards nur mit Hilfe einer Endomyokardbiopsie und einer anschließenden Histologie der entnommenen Probe möglich.
Wen kann ich kontaktieren?
Behandlung myokardiale Akinesie
Die Behandlung des Myokards zielt darauf ab, die Blutversorgung der geschädigten Bereiche (Perfusion) und ihre Leitungsfunktion wiederherzustellen, den Bereich der lokalisierten Kardiomyozytennekrose zu begrenzen und den Zellstoffwechsel zu aktivieren.
In der klinischen Praxis werden Medikamente verschiedener pharmakologischer Gruppen eingesetzt. Bei akuten Koronarsyndromen und okklusiver Thrombose der epikardialen Koronararterie wird eine Reperfusionstherapie mit Thrombolytika (Streptokinase, Prourokinase, Alteplase) und Thrombozytenaggregationshemmern (Ticlopidin, Clopidogrelsulfat oder Plavix) durchgeführt.
Bei chronischer Herzinsuffizienz werden Medikamente eingesetzt, die das Angiotensin-Converting-Enzym (ACE) hemmen, das den Blutdruck reguliert: Captopril, Enalapril, Ramipril, Fosinopril. Ihre Dosierung wird von einem Kardiologen in Abhängigkeit von der jeweiligen Erkrankung und den EKG-Werten festgelegt. Beispielsweise kann Captopril (Capril, Alopresin, Tensiomin) in einer Dosierung von 12,5–25 mg verschrieben werden – dreimal täglich vor den Mahlzeiten (oral oder unter der Zunge). Zu den Nebenwirkungen dieses Medikaments und der meisten Medikamente dieser Gruppe gehören Tachykardie, Blutdruckabfall, Nierenfunktionsstörungen, Leberversagen, Übelkeit und Erbrechen, Durchfall, Urtikaria, erhöhte Angstzustände, Schlaflosigkeit, Parästhesien und Tremor sowie Veränderungen der biochemischen Zusammensetzung des Blutes (einschließlich Leukopenie). Es ist zu beachten, dass ACE-Hemmer bei idiopathischen Myokarderkrankungen, Bluthochdruck, Stenose der Aorta und Nierengefäße, hyperplastischen Veränderungen der Nebennierenrinde, Aszites, Schwangerschaft und Kindheit nicht angewendet werden.
Bei koronarer Herzkrankheit und Kardiomyopathie können antiischämische Medikamente der Gruppe der peripheren Vasodilatatoren verschrieben werden, beispielsweise Molsidomin (Motazomin, Corvaton, Sidnofarm) oder Advocard. Molsidomin wird oral eingenommen – dreimal täglich eine Tablette (2 mg); kontraindiziert bei niedrigem Blutdruck und kardiogenem Schock; Nebenwirkung – Kopfschmerzen.
Das Antiarrhythmikum und Blutdrucksenker Verapamil (Veracard, Lekoptin) wird bei koronarer Herzkrankheit mit Tachykardie und Angina pectoris angewendet: dreimal täglich eine Tablette (80 mg). Nebenwirkungen können Übelkeit, Mundtrockenheit, Darmbeschwerden, Kopf- und Muskelschmerzen, Schlaflosigkeit, Urtikaria und Herzrhythmusstörungen sein. Dieses Medikament ist bei schwerer Herzinsuffizienz, Vorhofflimmern und Bradykardie sowie niedrigem Blutdruck kontraindiziert.
Das Medikament Mildronat (Meldonium, Angiocardil, Vasonat, Cardionat und andere Handelsnamen) hat eine kardiotonische und antihypoxische Wirkung. Es wird empfohlen, zweimal täglich eine Kapsel (250 mg) einzunehmen. Dieses Medikament darf nur von erwachsenen Patienten angewendet werden und ist bei zerebralen Durchblutungsstörungen und strukturellen Erkrankungen des Gehirns kontraindiziert. Bei der Anwendung von Mildronat können Nebenwirkungen wie Kopfschmerzen, Schwindel, Herzrhythmusstörungen, Kurzatmigkeit, Mundtrockenheit und Husten, Übelkeit und Darmbeschwerden auftreten.
Medikamente der β1-Adrenoblocker-Gruppe gegen koronare Herzkrankheit (Metoprolol, Propranolol, Atenolol, Acebutolol usw.) senken in erster Linie den Blutdruck und reduzieren durch die Verringerung der sympathischen Stimulation von Rezeptoren auf Myokardzellmembranen die Herzfrequenz, das Herzzeitvolumen, erhöhen den Sauerstoffverbrauch der Kardiomyozyten und lindern Schmerzen. Beispielsweise wird Metoprolol zweimal täglich eine Tablette verschrieben, bei Atenolol reicht eine Tablette täglich aus. Medikamente dieser Gruppe erhöhen jedoch das Risiko einer akuten Herzinsuffizienz sowie eines Vorhof- und Kammerblocks, und ihre Anwendung ist bei kongestiver und dekompensierter Herzinsuffizienz, Bradykardie und Kreislaufstörungen kontraindiziert. Daher stellen viele Experten derzeit die antiarrhythmische Wirkung dieser Medikamente in Frage.
Die Linderung von Herzschmerzen ist von größter Bedeutung, da die sympathische Aktivierung bei Schmerzen zu einer Verengung der Blutgefäße führt und die Belastung des Herzens erhöht. Nitroglycerin wird häufig zur Schmerzlinderung eingesetzt. Detaillierte Informationen finden Sie im Artikel - Wirksame Tabletten zur Linderung von Herzschmerzen
Ärzte empfehlen die Einnahme der Vitamine B6, B9 und E sowie zur Unterstützung des Reizleitungssystems des Herzens kalium- und manganhaltige Medikamente (Panangin, Asparkam usw.).
Chirurgische Behandlung
Bei Infarkten mit Schädigung der Koronararterien (was zur Bildung eines myokardialen Ischämiebereichs und seiner Akinese mit Erweiterung der Herzkammern führt) ist eine chirurgische Behandlung angezeigt, um den Blutfluss zum Herzen wiederherzustellen - ein aortokoronarer Bypass.
Bei einer ischämischen Herzkrankheit kommt eine Koronardilatation (Erweiterung des Lumens) zum Einsatz – das Stenting.
Bei dyskinetischen Aneurysmen wird am häufigsten eine chirurgische Behandlung angewendet: entweder durch Aneurysmektomie (Resektion), durch Nähen der Aneurysmahöhle (Aneurysmoplastik) oder durch Verstärkung ihrer Wand.
Es wurde eine Methode der dynamischen Kardiomyoplastie entwickelt, bei der die Myokardkontraktilität mithilfe eines elektrisch stimulierten Skelettmuskels (meist ein Lappen vom Rand des Latissimus dorsi-Muskels) wiederhergestellt oder verbessert wird, der um einen Teil des Herzens gewickelt wird (mit teilweiser Resektion der zweiten Rippe). Der Muskellappen wird um die Ventrikel genäht und seine synchrone Stimulation mit Herzkontraktionen erfolgt über intramuskuläre Elektroden eines implantierbaren Herzschrittmachers.
Verhütung
Kehren Sie zum Abschnitt Risikofaktoren zurück, und die Methoden zur Vorbeugung von Herz-Kreislauf-Erkrankungen werden deutlich. Die Hauptsache ist, nicht zuzunehmen, sich mehr zu bewegen und Cholesterin nicht in Form von Plaques an den Wänden der Blutgefäße absetzen zu lassen. Aus diesem Grund ist es nach 40 Jahren (und dem Vorhandensein von Herzerkrankungen bei Blutsverwandten) sinnvoll, die Diät gegen Arteriosklerose einzuhalten
Und natürlich betrachten Kardiologen die Raucherentwöhnung als die wichtigste Voraussetzung, um ischämischen Myokardschäden vorzubeugen. Tatsache ist, dass sich beim Rauchen die Hämoglobinproteine der roten Blutkörperchen mit den Gasen des inhalierten Tabakrauchs verbinden und eine für das Herz sehr schädliche Verbindung bilden – Carboxyhämoglobin. Diese Substanz verhindert den Sauerstofftransport der Blutzellen, was zu einer Hypoxie der Kardiomyozyten des Herzmuskels und zur Entwicklung einer Myokardischämie führt.
Lesen Sie auch – Prävention von Kardiosklerose nach einem Infarkt
Prognose
Kardiologen geben nur ungern Prognosen ab: Es ist schwierig, eine genaue Prognose der Dyskinesie, Hypokinesie und Akinesie nach einem Infarkt zu stellen.
Um die Sterblichkeitsprognose nach einem akuten Herzinfarkt einzuschätzen, haben Experten der American Society of Echocardiography den Wall Motion Index (WMI) eingeführt. Dieser hat jedoch keinen vollwertigen langfristigen Prognosewert.
Bei Myokarditis enden laut Statistik fast 30 % der Fälle mit einer Genesung, im übrigen wird eine chronische Dysfunktion des linken Ventrikels zur Komplikation. Darüber hinaus führen etwa 10 % der Fälle viraler und mikrobieller Myokarditis zum Tod der Patienten. Eine totale Myokardakinese führt zum Herzstillstand.

