
Alle iLive-Inhalte werden medizinisch überprüft oder auf ihre Richtigkeit überprüft.
Wir haben strenge Beschaffungsrichtlinien und verlinken nur zu seriösen Medienseiten, akademischen Forschungseinrichtungen und, wenn möglich, medizinisch begutachteten Studien. Beachten Sie, dass die Zahlen in Klammern ([1], [2] usw.) anklickbare Links zu diesen Studien sind.
Wenn Sie der Meinung sind, dass einer unserer Inhalte ungenau, veraltet oder auf andere Weise bedenklich ist, wählen Sie ihn aus und drücken Sie Strg + Eingabe.
Ösophagusatresie
Facharzt des Artikels
Zuletzt überprüft: 12.07.2025
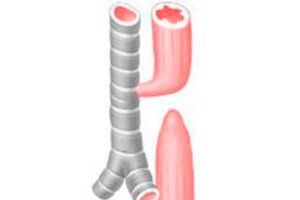
Bei der Ösophagusatresie (EA) handelt es sich um eine angeborene Fehlbildung, bei der die Speiseröhre etwa 8–12 cm vom Eingang der Mundhöhle entfernt blind endet.
Bei der angeborenen tracheoösophagealen Fistel ohne Atresie handelt es sich um einen pathologischen Kanal, der mit Granulationsgewebe oder Epithel ausgekleidet ist und das unveränderte Lumen der Speiseröhre mit dem Lumen der Luftröhre verbindet.
Die Ösophagusatresie ist die häufigste Form der Magen-Darm-Atresie.
Epidemiologie
Die Ösophagusatresie ist eine angeborene Fehlbildung des oberen Gastrointestinaltrakts mit einer geschätzten weltweiten Prävalenz von 1 zu 2.500 bis 1 zu 4.500 Geburten.[ 1 ] In den Vereinigten Staaten wird die Prävalenz auf 2,3 pro 10.000 Lebendgeburten geschätzt.[ 2 ] Die relative Inzidenz der Ösophagusatresie steigt mit dem Alter der Mutter.[ 3 ],[ 4 ]
Ursachen Ösophagusatresie
Die Ätiologie der Ösophagusatresie mit oder ohne assoziierte tracheoösophageale Fistel ist eine fehlende Teilung oder eine unvollständige Entwicklung des Vorderdarms.[ 5 ] Der Fistelgang entspringt einem Ast des embryonalen Lungenrudiments, der sich aufgrund mangelhafter epithelial-mesenchymaler Wechselwirkungen nicht verzweigt.
Mehrere Gene wurden mit Ösophagusatresie in Verbindung gebracht, darunter Shh, [ 6 ] SOX2, CHD7, MYCN und FANCB. Die Ätiologie ist jedoch noch nicht vollständig geklärt und wahrscheinlich multifaktoriell. Bei Patienten kann entweder eine isolierte AP/TPS oder ein Teil eines Syndroms wie VACTERL oder CHARGE diagnostiziert werden.
Pathogenese
Die Speiseröhre ist ein muskulärer Schlauch, der den Nahrungsbrei vom Rachen zum Magen transportiert. Sie entspringt der Keimschicht des Endoderms, die wiederum Rachen, Speiseröhre, Magen und die Epithelschichten des Aerodigestivtrakts bildet. Trachea und Speiseröhre entstehen durch die Teilung eines gemeinsamen Vorderdarms in der frühen fetalen Entwicklung. [ 7 ] Wird dieser gemeinsame Vorderdarm nicht vollständig geteilt oder entwickelt, kann dies zu einer Ösophagotrachealfistel (TEF) und Ösophagusatresie (EA) führen. Pränatal können Patienten mit Ösophagusatresie ein Polyhydramnion aufweisen, vorwiegend im dritten Trimenon, was ein diagnostischer Hinweis auf eine Ösophagusatresie sein kann.
Darüber hinaus weisen etwa 50 % der Patienten mit TPS/EA damit verbundene angeborene Anomalien auf, darunter VACTERL (Wirbeldefekte, Analatresie, Herzfehler, Ösophagotrachealfistel, Nierenanomalien und Gliedmaßenanomalien) oder CHARGE ( Kolobom, Herzfehler, Choanalatresie, Wachstumsverzögerung, Genitalanomalien und Ohranomalien). Nach der Geburt des Neugeborenen sind die häufigsten Symptome einer Ösophagusatresie übermäßiger Speichelfluss, Würgen und die Unfähigkeit, eine Magensonde einzuführen. Darüber hinaus kommt es bei einem assoziierten TPS zu einer Magenblähung, da Luft von der Trachea durch die distale Ösophagusfistel in den Magen gelangt.
Patienten mit diesem Symptomkomplex sollten einer beschleunigten Untersuchung auf Ösophagusatresie und tracheoösophageale Fistel unterzogen und umgehend zur Untersuchung durch einen Kinderchirurgen an eine Einrichtung höherer Versorgungsstufe überwiesen werden.
Pathophysiologie
Tracheoösophageale Fistel und Ösophagusatresie entstehen durch eine fehlerhafte laterale Unterteilung des Vorderdarms in Speiseröhre und Trachea. Der Fistelgang zwischen Speiseröhre und Trachea kann sich sekundär aufgrund fehlerhafter epithelial-mesenchymaler Interaktionen bilden. [6] Tracheoösophageale Fistel und Ösophagusatresie treten in etwa 90 % der Fälle gemeinsam auf. Ösophagusatresie und tracheoösophageale Fistel werden anhand ihrer anatomischen Konfiguration in fünf Kategorien eingeteilt. [ 8 ]
- Typ A ist eine isolierte Ösophagusatresie ohne assoziierte tracheoösophageale Fistel, deren Prävalenz 8 % beträgt.
Der proximale und distale Ösophagus enden blind und sind nicht mit der Trachea verbunden. Der proximale Ösophagus ist dilatiert, dickwandig und endet meist höher im hinteren Mediastinum, nahe dem zweiten Brustwirbel. Der distale Ösophagus ist kurz und endet in unterschiedlichem Abstand zum Zwerchfell. Der Abstand zwischen den beiden Enden bestimmt, ob eine primäre Rekonstruktion möglich ist (selten) oder ob eine verzögerte primäre Anastomose oder ein Ösophagusersatz durchgeführt werden sollte. In diesen Fällen ist es wichtig, eine proximale tracheoösophageale Fistel auszuschließen.
- Typ B ist eine Ösophagusatresie mit proximaler tracheoösophagealer Fistel. Mit einer Prävalenz von 1 % ist dies der seltenste Typ.
Diese seltene Anomalie muss von der isolierten Variante unterschieden werden. Die Fistel befindet sich nicht am distalen Ende des oberen Sacks, sondern 1–2 cm oberhalb seines Endes an der Vorderwand der Speiseröhre.
- Die Ösophagusatresie Typ C ist die häufigste (84–86 %) und umfasst eine proximale Ösophagusatresie mit distaler tracheoösophagealer Fistel.
Es handelt sich um eine Atresie, bei der der proximale Ösophagus erweitert und die Muskelwand verdickt ist. Er endet blind im oberen Mediastinum etwa auf Höhe des dritten oder vierten Brustwirbels. Der distale Ösophagus, der dünner und schmaler ist, tritt an der Carina oder häufiger ein bis zwei Zentimeter proximal der Trachea in die hintere Wand der Trachea ein. Der Abstand zwischen dem blinden proximalen Ösophagus und der distalen tracheoösophagealen Fistel variiert von überlappenden Segmenten bis hin zu einem breiten Schlitz. Sehr selten kann die distale Fistel verschlossen oder obliteriert sein, was vor der Operation zu einer Fehldiagnose einer isolierten Atresie führen kann.
- Typ D - Ösophagusatresie mit proximaler und distaler tracheoösophagealer Fistel, selten - etwa 3%
Bei vielen dieser Säuglinge wurde die Anomalie fälschlicherweise als proximale Atresie und distale Fistel diagnostiziert. Aufgrund wiederkehrender Atemwegsinfektionen wurde bei der Untersuchung eine tracheoösophageale Fistel festgestellt, die zuvor mit einer rezidivierenden Fistel verwechselt wurde. Durch die zunehmende präoperative Endoskopie (Bronchoskopie und/oder Ösophagoskopie) kann die „doppelte“ Fistel frühzeitig erkannt und im Rahmen des ersten Eingriffs vollständig versorgt werden. Wird eine proximale Fistel präoperativ nicht identifiziert, sollte die Diagnose durch ein großes Gasleck aus dem oberen Beutel während der Anastomose vermutet werden.
- Bei der Ösophagusatresie Typ E handelt es sich um eine isolierte tracheoösophageale Fistel ohne assoziierte Ösophagusatresie. Sie wird als Typ „H“ bezeichnet und hat eine Prävalenz von etwa 4 %.
Zwischen der anatomisch intakten Speiseröhre und der Trachea besteht eine Fistelverbindung. Der Fistelgang kann sehr eng sein (3–5 mm Durchmesser) und befindet sich meist im unteren Halsbereich. Es handelt sich meist um einzelne Fisteln, es wurden jedoch auch zwei oder sogar drei Fisteln beschrieben.
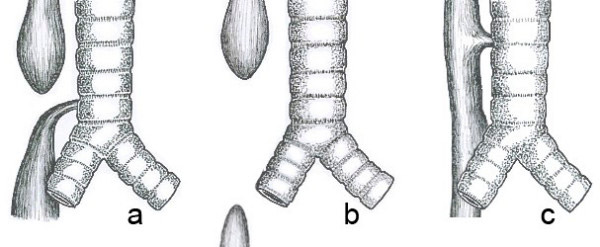
Häufige anatomische Formen der Ösophagusatresie: a) Ösophagusatresie mit distaler Ösophagotrachealfistel (86 %), b) Isolierte Ösophagusatresie ohne Ösophagotrachealfistel (7 %), c) Ösophagotrachealfistel vom H-Typ (4 %)
Symptome Ösophagusatresie
Bei etwa einem Drittel der Feten werden Ösophagusatresie und Ösophagotrachealfistel pränatal diagnostiziert. Das häufigste sonographische Zeichen einer Ösophagusatresie ist ein Polyhydramnion, das bei etwa 60 % der Schwangerschaften auftritt. [ 9 ] Bei einer pränatalen Diagnose kann die Familie über die postnatalen Erwartungen beraten werden.
In vielen Fällen wird die Diagnose jedoch erst bei der Geburt gestellt. Säuglinge mit Ösophagusatresie zeigen kurz nach der Geburt Symptome wie erhöhte Sekrete, die zu Erstickungsanfällen, Atemnot oder Zyanose-Episoden beim Stillen führen. Bei einer Ösophagusatresie führt eine Fistel zwischen der Luftröhre und dem distalen Ösophagus dazu, dass sich der Magen im Röntgenbild des Brustkorbs mit Gas füllt. Säuglinge mit Ösophagusatresie Typ A und B haben keine Bauchblähung, da keine Fistel von der Luftröhre zum distalen Ösophagus besteht. Bei Säuglingen mit einer tracheoösophagealen Fistel kann Mageninhalt durch die Fistel in die Luftröhre zurückfließen, was zu Aspirationspneumonie und Atemnot führt. Bei Patienten mit Ösophagusatresie Typ E kann sich die Diagnose verzögern, wenn die Fistel klein ist.[ 10 ]
Wo tut es weh?
Was bedrückt dich?
Formen
Es gibt etwa 100 bekannte Varianten dieses Defekts, aber drei der häufigsten sind:
- Ösophagusatresie und Fistel zwischen distaler Speiseröhre und Luftröhre (86-90%),
- isolierte Ösophagusatresie ohne Fistel (4-8%),
- Tracheoösophageale Fistel, Typ H (4 %).
In 50–70 % der Fälle einer Ösophagusatresie liegen kombinierte Entwicklungsstörungen vor:
- angeborene Herzfehler (20-37%),
- Defekte des Magen-Darm-Trakts (20-21%),
- Defekte des Urogenitalsystems (10%),
- Muskel-Skelett-Defekte (30%),
- kraniofaziale Defekte (4%).
In 5–7 % der Fälle geht die Ösophagusatresie mit Chromosomenanomalien (Trisomie 18, 13 und 21) einher. Eine besondere Kombination von Entwicklungsstörungen bei Ösophagusatresie wird als „VATER“ bezeichnet, wobei die lateinischen Anfangsbuchstaben der folgenden Entwicklungsdefekte (5–10 %) verwendet werden:
- Wirbelsäulendefekte (V),
- Analdefekte (A),
- tracheoösophageale Fistel (T),
- Ösophagusatresie (E),
- Radiusknochendefekte (R).
30-40% der Kinder mit Ösophagusatresie sind Frühgeburten oder haben eine intrauterine Wachstumsverzögerung. [ 11 ], [ 12 ]
Komplikationen und Konsequenzen
Nach der Reparatur einer Ösophagusatresie können chirurgische Komplikationen auftreten. Die am meisten gefürchtete Komplikation ist eine Ösophagusanastomoseninsuffizienz.[ 13 ] Kleinere Leckagen können mit einer Thoraxdrainage und verlängerter NPO behandelt werden, bis die Leckage behoben ist. Bei größeren Leckagen oder einer Anastomoseninsuffizienz kann eine erneute Operation und eine Ösophagusresektion mit Zwischenschaltung eines Magen-, Kolon- oder Jejunumtransplantats erforderlich sein.
Eine weitere mögliche Komplikation ist eine Ösophagusanastomosenstriktur. Diese wird üblicherweise mit seriellen endoskopischen Ösophagusdilatationen behandelt.[ 14 ] Schließlich wurde, wenn auch selten, über wiederkehrende Fistelbildungen in Speiseröhre und Luftröhre berichtet. Diese Probleme werden mit einer erneuten Operation behandelt.
Nichtchirurgische Komplikationen bei Ösophagusatresie und tracheoösophagealer Fistel sind häufig. Die Anwendung von Protonenpumpenhemmern wird für mindestens ein Jahr nach der Behandlung einer Ösophagusatresie aufgrund einer Ösophagusmotilitätsstörung empfohlen, die zu einem erhöhten gastroösophagealen Reflux (GER) und einem erhöhten Aspirationsrisiko führt.[ 15 ] Tracheomalazie tritt häufig nach Operationen auf. Neugeborene mit Ösophagusatresie und tracheoösophagealer Fistel weisen typischerweise eine erhöhte Inzidenz von Dysphagie, Atemwegsinfektionen und Ösophagitis auf.[ 16 ]
Aufgrund erhöhter GER-Werte im Kindes- und Erwachsenenalter haben diese Kinder im Vergleich zur Allgemeinbevölkerung eine höhere Inzidenz von Barrett-Ösophagus und ein höheres Risiko für Speiseröhrenkrebs.[17 ] Für diese Patienten werden Screening-Protokollefür Speiseröhrenkrebs empfohlen, obwohl dies umstritten ist.
Diagnose Ösophagusatresie
Eine Ösophagusatresie wird in der Regel diagnostiziert, wenn eine Magensonde nicht eingeführt werden kann. Die Sonde reicht nicht bis zum Magen und kann auf einem Röntgenbild des Thorax oberhalb der Ösophagusatresie gewunden sein. Die endgültige Diagnose kann durch Injektion einer kleinen Menge wasserlöslichen Kontrastmittels in die Magensonde unter Röntgenkontrolle gestellt werden. Barium sollte vermieden werden, da es bei Aspiration in die Lunge eine chemische Pneumonitis verursachen kann.Eine Ösophagoskopie oder Bronchoskopie zum Nachweis einer Trachealfistel kann zur Bestätigung der Diagnose eingesetzt werden.[ 18 ]
Bei Neugeborenen mit Ösophagusatresie und Ösophagotrachealfistel muss auf VACTERL- und CHARGE-Anomalien untersucht werden, da diese bei bis zu 50 % der Neugeborenen auftreten können. Für eine vollständige Untersuchung sind insbesondere ein Herzechokardiogramm, Röntgenaufnahmen der Extremitäten und der Wirbelsäule, eine Ultraschalluntersuchung der Nieren und eine gründliche körperliche Untersuchung von After und Genitalien auf Anomalien erforderlich. Im Rahmen einer großen monozentrischen Studie in den USA wurden die am häufigsten auftretenden angeborenen Anomalien in Zusammenhang mit Ösophagusatresie und Ösophagotrachealfistel untersucht. Unter den fast 3.000 Patienten umfassten die assoziierten VACTERL-Diagnosen bei 25,5 % Wirbelsäulenanomalien, bei 11,6 % anorektale Fehlbildungen, bei 59,1 % angeborene Herzfehler, bei 21,8 % Nierenerkrankungen und bei 7,1 % Gliedmaßendefekte. [ 19 ] Fast ein Drittel hatte 3 oder mehr Anomalien und erfüllte die Kriterien für eine VACTERL-Diagnose.
Was muss untersucht werden?
Wie zu prüfen?
Differenzialdiagnose
Zu den Differentialdiagnosen zählen Kehlkopf-, Tracheal- und Speiseröhrenspalten, Ösophagussepten oder -ringe, Ösophagusstrikturen, tubuläre Ösophagusduplikationen, angeborene verkürzte Speiseröhre und Tracheaagenesie. Diese Diagnosen können mithilfe verschiedener bildgebender Verfahren – von Röntgen- und CT-Aufnahmen bis hin zu Endoskopie und chirurgischen Eingriffen – weiter untersucht werden.
Wen kann ich kontaktieren?
Behandlung Ösophagusatresie
Sobald die Diagnose einer Ösophagusatresie gestellt ist, sollte der Säugling intubiert werden, um die Atemwege zu kontrollieren und eine weitere Aspiration zu verhindern. Falls noch nicht geschehen, sollte vorsichtig ein Katheter eingeführt werden, um oropharyngeale Sekrete abzusaugen. Der Säugling sollte Antibiotika und intravenöse Flüssigkeit erhalten und darf nicht oral aufgenommen werden. Eine totale parenterale Ernährung (TPN) sollte für den Säugling in Betracht gezogen werden. Sobald der Säugling hämodynamisch stabilisiert ist und die Atemwege stabilisiert sind, sollte ein Kinderchirurg konsultiert werden.
Der Zeitpunkt der endgültigen chirurgischen Behandlung einer Ösophagusatresie hängt von der Größe des Säuglings ab. Wiegt der Säugling mehr als 2 Kilogramm, wird eine Operation in der Regel nach Korrektur etwaiger Herzfehler angeboten. Säuglinge mit sehr geringem Geburtsgewicht (<1500 Gramm) werden in der Regel schrittweise behandelt, wobei zunächst die Fistel ligiert wird und anschließend mit zunehmendem Wachstum des Säuglings die Ösophagusatresie korrigiert wird.[ 20 ]
Zu den chirurgischen Optionen zur Reparatur einer Ösophagusatresie gehören die offene Thorakotomie oder die videoassistierte thorakoskopische Operation.[ 21 ] Die Schritte sind bei beiden Operationen gleich. Die Fistel zwischen Speiseröhre und Luftröhre wird identifiziert und durchtrennt. Ein Bronchoskop kann verwendet werden, um den Ursprung der Fistel in der Luftröhre sichtbar zu machen. Sobald die Fistel unterbunden ist, wird die Ösophagusatresie repariert. Typischerweise wird eine kleine Magensonde so gelegt, dass sie die beiden Enden kreuzt, und die Enden werden mit resorbierbarem Nahtmaterial vernäht, wenn sie ohne zu große Spannung erreicht werden können. Wenn die Enden der Speiseröhre zu stark gespannt sind oder nicht erreicht werden können, kann die Foker-Technik angewendet werden.[ 22 ] Bei dieser Technik werden Zugnähte an den Enden der Speiseröhre verwendet und diese langsam zusammengeführt. Sobald die Enden spannungsfrei zusammenkommen, kann die primäre Reparatur durchgeführt werden.
Liegt ein besonders langer Riss der Speiseröhre vor, der eine primäre Anastomose ausschließt, kann die Einfügung eines anderen Organs wie Magen, Dickdarm oder Jejunum erfolgen.[ 23 ] Patienten mit einer Ösophagusatresie vom Typ E (H-Typ) können mit einer hohen zervikalen Inzision behandelt werden und vermeiden so eine Thorakotomie zur Fistelligatur.[ 24 ] Eine Gastrostomie ist in der Regel nicht angezeigt, es sei denn, die primäre Anastomose ist fehlgeschlagen.
Nach der Operation wird das Kind zur genauen Beobachtung auf die Neugeborenen-Intensivstation zurückgebracht. Ein Thoraxröhrchen verbleibt auf der Seite des Brustzugangs. Das Kind wird weiterhin parenteral über eine Magensonde ernährt und intermittiert abgesaugt. Nach 5 bis 7 Tagen wird eine Ösophagographie durchgeführt, um auf Leckagen in der Speiseröhre zu prüfen. Wird kein Leck gefunden, wird in der Regel mit der oralen Ernährung begonnen. Liegt ein Leck vor, sammelt das Thoraxröhrchen den Ausfluss. Das Thoraxröhrchen verbleibt, bis das Leck verschlossen ist und/oder das Kind die orale Ernährung toleriert.
Prognose
Die Prognose für Neugeborene mit Ösophagusatresie und tracheoösophagealer Fistel ist relativ gut und hängt hauptsächlich von den Herz- und Chromosomenanomalien und nicht von der Ösophagusatresie selbst ab. Die Gesamtüberlebensrate liegt im Allgemeinen bei 85–90 %. [ 25 ] Eine höhere Mortalität wird beobachtet, wenn neben der Ösophagusatresie auch Herzanomalien vorliegen. Frühe Todesfälle sind mit Herzanomalien assoziiert, während späte Todesfälle mit Atemwegskomplikationen einhergehen. Der Abstand zwischen den beiden Ösophagustaschen, insbesondere wenn dieser groß ist, kann die Prognose bestimmen. [ 26 ] Alle Neugeborenen, die sich einer Ösophagusatresie unterziehen, haben erwartungsgemäß Magen-Darm- und Atemprobleme, die sich in der Regel mit zunehmendem Alter bessern.
Quellen
- Nasr T, Mancini P, Rankin SA, Edwards NA, Agricola ZN, Kenny AP, Kinney JL, Daniels K, Vardanyan J, Han L, Trisno SL, Cha SW, Wells JM, Kofron MJ, Zorn AM. Endosomenvermittelte epitheliale Umgestaltung nach Hedgehog-Gli ist für die tracheoösophageale Trennung erforderlich. Dev Cell. 16. Dezember 2019;51(6):665-674.e6.
- Pretorius DH, Drose JA, Dennis MA, Manchester DK, Manco-Johnson ML. Tracheoösophageale Fistel in der Gebärmutter. 22 Fälle. J Ultrasound Med. 1987 Sep;6(9):509-13.
- Cassina M, Ruol M, Pertile R, Midrio P, Piffer S, Vicenzi V, Saugo M, Stocco CF, Gamba P, Clementi M. Prävalenz, Merkmale und Überleben von Kindern mit Ösophagusatresie: Eine 32-jährige bevölkerungsbasierte Studie mit 1.417.724 aufeinanderfolgenden Neugeborenen. Birth Defects Res A Clin Mol Teratol. 2016 Jul;106(7):542-8.
- Karnak I, Senocak ME, Hiçsönmez A, Büyükpamukçu N. Diagnose und Behandlung der tracheoösophagealen Fistel vom H-Typ. J Pediatr Surg. 1997 Dez;32(12):1670-4.
- Scott DA Übersicht über Ösophagusatresie / Ösophagotrachealfistel – Ausgemustertes Kapitel, nur als historische Referenz. In: Adam MP, Feldman J, Mirzaa GM, Pagon RA, Wallace SE, Bean LJH, Gripp KW, Amemiya A, Hrsg. GeneReviews® [Internet]. University of Washington, Seattle; Seattle (WA): 12. März 2009.
- Crisera CA, Grau JB, Maldonado TS, Kadison AS, Longaker MT, Gittes GK. Defekte epithelial-mesenchymale Interaktionen bestimmen die Organogenese der tracheoösophagealen Fistel. Pediatr Surg Int. 2000;16(4):256-61.
- Spitz L. Ösophagusatresie. Orphanet J Rare Dis. 11. Mai 2007;2:24.
- Lupo PJ, Isenburg JL, Salemi JL, Mai CT, Liberman RF, Canfield MA, Copeland G, Haight S, Harpavat S, Hoyt AT, Moore CA, Nembhard WN, Nguyen HN, Rutkowski RE, Steele A, Alverson CJ, Stallings EB, Kirby RS. und das National Birth Defects Prevention Network. Bevölkerungsbasierte Daten zu Geburtsfehlern in den USA, 2010–2014: Ein Schwerpunkt auf gastrointestinalen Defekten. Birth Defects Res. 2017 Nov 01;109(18):1504–1514.
- Clark DC. Ösophagusatresie und tracheoösophageale Fistel. Am Fam Physician. 15. Februar 1999;59(4):910-6, 919-20.
- Lautz TB, Mandelia A, Radhakrishnan J. VACTERL-Assoziationen bei Kindern, die sich einer Operation wegen Ösophagusatresie und anorektaler Fehlbildungen unterziehen: Auswirkungen für Kinderchirurgen. J Pediatr Surg. 2015 Aug;50(8):1245-50.
- Petrosyan M, Estrada J, Hunter C, Woo R, Stein J, Ford HR, Anselmo DM. Ösophagusatresie/tracheoösophageale Fistel bei Neugeborenen mit sehr geringem Geburtsgewicht: Verbesserte Ergebnisse durch schrittweise Reparatur. J Pediatr Surg. 2009 Dez;44(12):2278-81.
- Patkowsk D, Rysiakiewicz K, Jaworski W, Zielinska M, Siejka G, Konsur K, Czernik J. Thorakoskopische Reparatur einer tracheoösophagealen Fistel und einer Ösophagusatresie. J Laparoendosc Adv Surg Tech A. 2009 Apr;19 Suppl 1:S19-22.
- Foker JE, Linden BC, Boyle EM, Marquardt C. Entwicklung einer echten Primärreparatur für das gesamte Spektrum der Ösophagusatresie. Ann Surg. 1997 Okt;226(4):533-41; Diskussion 541-3.
- Bairdain S, Foker JE, Smithers CJ, Hamilton TE, Labow BI, Baird CW, Taghinia AH, Feins N, Manfredi M, Jennings RW. Jejunale Interposition nach fehlgeschlagener Ösophagusatresie-Reparatur. J Am Coll Surg. 2016 Jun;222(6):1001-8.
- Ko BA, Frederic R, DiTirro PA, Glatleider PA, Applebaum H. Vereinfachter Zugang zur Teilung der tiefen zervikalen/hohen thorakalen H-Typ-Tracheoösophagealfistel. J Pediatr Surg. 2000 Nov;35(11):1621-2. [PubMed]
- 16.
- Choudhury SR, Ashcraft KW, Sharp RJ, Murphy JP, Snyder CL, Sigalet DL. Überleben von Patienten mit Ösophagusatresie: Einfluss von Geburtsgewicht, Herzanomalie und späten Atemwegskomplikationen. J Pediatr Surg. 1999 Jan;34(1):70-3; Diskussion 74.
- Upadhyaya VD, Gangopadhyaya AN, Gupta DK, Sharma SP, Kumar V, Pandey A, Upadhyaya AD. Prognose einer angeborenen tracheoösophagealen Fistel mit Ösophagusatresie anhand der Spaltlänge. Kinderchirurg Int. 23. August 2007 (8): 767-71.
- Engum SA, Grosfeld JL, West KW, Rescorla FJ, Scherer LR. Analyse der Morbidität und Mortalität in 227 Fällen von Ösophagusatresie und/oder tracheoösophagealer Fistel über zwei Jahrzehnte. Arch Surg. 1995 Mai;130(5):502-8; Diskussion 508-9.
- Antoniou D, Soutis M, Christopoulos-Geroulanos G. Anastomosenstrikturen nach Ösophagusatresie-Reparatur: 20 Jahre Erfahrung mit endoskopischer Ballondilatation. J Pediatr Gastroenterol Nutr. 2010 Okt;51(4):464-7.
- Krishnan U, Mousa H, Dall'Oglio L, Homaira N, Rosen R, Faure C, Gottrand F. ESPGHAN-NASPGHAN-Leitlinien zur Beurteilung und Behandlung gastrointestinaler und ernährungsbedingter Komplikationen bei Kindern mit Ösophagusatresie-Tracheoösophagealfistel. J Pediatr Gastroenterol Nutr. 2016 Nov;63(5):550-570.
- Connor MJ, Springford LR, Kapetanakis VV, Giuliani S. Ösophagusatresie und Übergangsversorgung – Schritt 1: Eine systematische Überprüfung und Metaanalyse der Literatur zur Bestimmung der Prävalenz chronischer Langzeitprobleme. Am J Surg. 2015 Apr;209(4):747-59.
- Jayasekera CS, Desmond PV, Holmes JA, Kitson M, Taylor AC. Cluster von 4 Fällen von Plattenepithelkarzinomen der Speiseröhre bei Erwachsenen mit chirurgisch korrigierter Ösophagusatresie – Zeit für den Beginn des Screenings. J Pediatr Surg. 2012 Apr;47(4):646-51.

